“Si Déu ha concebut el llamp per castigar els homes, Déu ha estat vençut per Benjamí Franklin”. Aquesta citació de Joan Salvat-Papasseit expressa com el camí de la tècnica i de la ciència obliga la teologia a qüestionar-se les representacions divines. Zeus, el Déu del Tron, resol no pocs conflictes amb un llamp que fulmina tots aquells que trenquen, voluntàriament o involuntària, l’ordre natural, el cosmos, com s’esdevé amb Faetó o amb Asclepi. Els antics déus foren bandejats amb el triomf del cristianisme, que els condensà tots en un Déu únic i tri, Pare, Fill i Esperit Sant. El cristianisme, nascut com una secta jueva, va fer de la setmana, el cicle de set dies, la base del seu ritual. A l’Antiga Roma, havia existit un cicle semblant, normalment de vuit dies, de manera que set dies separaven el “nundinum”, o dia de mercat. Aquest cicle es va transformar en un de set, encara en època precristiana, i ja en el segle II tenim una adscripció divina. En el còmput actual, hom sol començar la setmana en el “dies Lunae”, és a dir el dilluns, de manera que el dia queda just en el mig del cicle és el “dies Iovis”, és a dir el dijous. En el Jou de dijous homenatgem al Pare de tots els Déus, per bé que ja tinguem explicat meteorològicament l’origen dels llamps i trons. En alemany, “dijous” és “Donnerstag”, literalment el dia del Tro. En les llengües escandinaves i en anglès modern, hom fa un pas més i “dijous” és “Torsdag” o “Thursday”, literalment el dia del Thor. Certament, el nom de Donar i Thor comparteixen el mateix origen en “*þunraz” que vol dir senzillament tro i que és alhora el nom d’una divinitat. La identificació entre Thor i Júpiter/Zeus no és pas unànime. Tàcit havia identificar Donar/Thor amb Heracles, i ho havia fet per dues raons. Thor és un Déu Fill, com Hèrcules, i si Thor té associat el Martell, Hèrcules té associada el Bastó. És clar, que el pare de Thor és Odin/Wotan, que Tàcit identifica amb Hermes. Fins i tot assumint un origen comú protoindogermànic d’aquestes divinitats, cal tenir present l’evolució de les creences. En el 1962, per exemple, Thor és reciclat per Stan Lee per a Marvel Comics com un superheroi. En efecte, Odin havia fet reencarnar el seu fill Thor en un estudiant de medicina discapacitat anomenat Donald Blake.

“Tors strid med jättarna”, Tor lluita amb gegants, pintura de 1872, de Mårten Eskil Winge (1825-1896). Thor, originari del món dels déus (Asgard) és alhora protector del món dels homes (Midgard). La mitologia nòrdica preveia un Gotterdammerung, que alguns missioners van voler identificar amb el Triomf del Cristianisme. Així, els missioners presentaren Thor i els altres déus com “dimonis”. En el segle XIX, Thor i el panteó nòrdic serà objecte d’inspiració artística per als pobles germànics
Jöns Jacob Berzelius i la descoberta del tori

En el 1828 arribà a les mans de Jöns Jacob Berzelius (1779-1848), secretari de la Reial Acadèmica Sueca de Ciència un mineral rar de color negre. El trametia Jens Esmark, professor de mineralogia i geologia a la Universitat de Cristiania (Oslo), que, al seu torn, l’havia rebut del seu fill, Hans Morten Thrane Esmark (1801-1882). El jove Esmark les havia pres a Løvøya, una petita illa de l’Ormefjorden, una branca del Breviksfjorden, en Telemark. Precisament, el jove Esmarck era vicari a Brevik, i aprofitava els temps lliures per aplegar una col•lecció de minerals, en la línia del seu pare i de l’avi matern (Morten Thrane Brünnich, traspassat en 1827).

Espècimens de torita, procedents de Langesund i Arendal
Berzelius analitzà la composició del mineral, i trobà una terra que podria correspondre’s a un element químic prèviament desconegut. Per a l’element proposà el nom de “thorium” (tori), en honor de la divinitat escandinava. En correspondència, la terra rebria el nom de “tòria” i el mineral el nom de torita.
No era la primera vegada que Berzelius emprava el mot “tori” per referir-se a un element químic hipotètic. Ja ho havia fet en el 1815, quan analitzava un mineral procedent de la mina de coure de Falun (Dalarna, Suècia). L’anàlisi posterior, fet per ell mateix, el va obligar a desdir-se’n, ja que el compost de “tori” en qüestió era en realitat ortofosfat d’itri. Com a signe de penitència, Berzelius va denominar el mineral com a “kenotime”, a partir dels mots grecs κενός (buit) i τιμή (honor), en el sentit de “honor buit”. Per un error tipogràfic, “kenotime” es convertí en “xenotime” (“honor estrany”), i així quedà denominat el dit mineral.
Ara, però, Berzelius era més segur de la identificació. A diferència del xenotim, que era un mineral fosfat, la torita era un silicat de tori i d’urani. En el 1829, Berzelius publicà un article en la revista de la Reial Acadèmia (“Undersökning af ett nytt mineral (Thorit), som innehåller en förut obekant jord”) i un altre a Annalen der Physik und Chemie. En aquests reports, Berzelius resumia les característiques del mineral, el procés d’extracció de la terra i la seva reactivitat química.
Com a símbol químic del tori s’adoptaren les inicials del mot llatí, Th.
En el 1851, C. Bergermann va descriure en mostres d’orangita de Langesundfjord (prop de Brevik) un nou element, que suposà diferent del tori. Li va donar el nom de “donarium” (donari; en referència a Donar, la versió germànica del Thor nòrdic). Investigacions posteriors mostraren la identitat del donari i del tori.
En el 1862, J. F. Bahr descrigué en mostres de wasita procedents de Rösholm (prop d’Estocolm) la presència d’un nou òxid metàl•lic. Denominà l’element amb el nom de “wasium” (vasi). Bahr es retractà l’any següent, i estudis ulteriors indiquen que el vasi era en realitat tori.
En algunes llistes, el tori apareixia com el més pesant dels elements químics. Per exemple, en l’intent de sistematització dels elements químics de John Newlands (1864), el tori apareix en el darrer lloc, amb el nombre 56, adscrit en conseqüència al grup de l’oxigen, en el qual predominarien elements divalents com el mateix tori.
En la taula periòdica del 1869, Dmitri Mendeleev assigna temptativament al tori un pes atòmic força inferior, de 118 (“Th = 118?”). Això el col•locaria en el quart període, en un grup en el qual assenyala, també temptativament, l’indi com a element del tercer període.
En canvi, en la taula periòdica del 1871, Dmitri Mendeleev assigna al tori un pes atòmic de 231, la qual cosa el faria l’element conegut més pesant de tots, amb l’excepció de l’urani (U = 240). Mendeleev en aquesta taula situa el tori en la dotzena sèrie, dins del grup IV (el grup del carboni), assenyalant que és un element tetravalent. En dissenys ulteriors, el tori apareix ja definitivament en el setè període, però la seva classificació grupal serà encara matèria de discussió. El grup IV era escindit per alguns autors en un IVa (grup del titani) i un IVb (grup de l’oxigen), i s’entenia que el tori era el representant del setè període d’aquest grup IVa. En el 1892, en canvi, hom havia proposat que els elements transbismutians, inclòs el tori, fossin considerats com un bloc diferenciat en la taula periòdica.
En el 1890, Carl Auer von Welsbach (1858-1929) trobà la primera aplicació industrial d’un compost de tori. Welsbach, expert en elements de terres rares, havia patentat en el 1885 una manta incandescent amb el nom d’Actinophor, feta d’òxid de magnesi (60%), òxid de lantà (20%) i òxid d’itri (20%). En el 1887 l’havia començat a comercialitzar, però la llum emetia, massa verdosa, no fou gaire ben rebuda, i la fàbrica que havia establert Atzgersdorf va haver de plegat. Welsbach trobà que l’òxid de tori era millor que no pas la barreja de l’Actinophor. Certament, l’òxid de tori, escalfat, emet una llum blava intensa, però que es pot fer blanca si s’hi afegeixen quantitats d’òxid de ceri. Així formulà en 1891 una nova manta amb un 99% d’òxid de tori i un 1% d’òxid de ceri, que oferia una llum molt més blanca. En el 1892 la començà a fabricar, amb un notable èxit, particularment en l’ús per a enllumenat urbà, on tan sols cediria el lloc a l’enllumenat elèctric.

Llum emesa per mantes incandescents d’òxid de tori
En el 1898, Marie Sklodowska Curie (1867-1934) mostrava que la radioactivitat detectada en compostos d’urani també era una propietat de compostos de tori. De manera independent a Curie, Gerhard Carl Schmidt (1865-1949) havia detectat igualment radioactivitat en tori i en compostos de tori, i en publicà un article a Annalen der Physik.
Entre el 1900 i el 1903, Ernest Rutherford (1871-1937) i Frederick Soddy (1877-1956) determinaren que les radiacions de tori eren una propietat intrínseca. Van identificar els diferents productes en el qual dequeia el tori: tori-A (ThA), tori-B (ThB), tori-C (ThC), tori-C’ (ThC’), tori-C’’ (ThC’’) i tori-D (ThD). Rutherford també va descriure una substància radioactiva, emesa per compostos de tori, a la que denominà “emanació de tori” (ThEm) o “toró” (Tn).
En el 1905, Otto Hahn (1879-1968) identifica una fracció del tori molt més radioactiva, a la que denominà radiotori (RdTh). Hom també identificà un precursor del tori, amb el nom de mesotori (MsTh), que fou subdividit després en dues substàncies diferents, el mesotori-1 (MsTh1) i el mesotori-2 (MsTh2). Hahn proposà unes noves denominacions més senzilles: tori-1 (per comptes de mesotori-1), tori-2 (per comptes de mesotori-2) i tori-3 (per comptes de radiotori).
En el 1906, Hahn identificà el radioactini, com una fracció de l’actini més radioactiva.
En el 1908, Bertram B. Boltwood (1870-1927) va detectar una substància radioactiva en minerals d’urani, que considerà que podia ser un nou element químic. El batejà amb el nom de “ionium” (ioni) i l’assignà el símbol químic Io, bo i remarcant unes propietats químiques similars a les del tori.
En el 1908, Baskerville, de la University of North Carolina, proposà que el tori era en realitat una barreja de dos elements. Baskerville descartà conservar el nom de tori, i emprà per als dos elements els noms, respectivament, de carolini (en homenatge a les Carolines) i de berzeli (en homenatge a Berzelius). Aquesta descoberta no fou acceptada.

En la revista Popular Science, en 1909, proposaven l’experiment de col•locar una manta incandescent damunt de llavors i observar els efectes de la radioactivitat de l’òxid de tori de la manta en les plantes resultants. Algunes opinions de l’època sostenien un efecte “fertilitzant” de les radiacions i d’altres les consideraven detrimentals.
En el 1911, Antonoff descrigué l’urani Y com a producte de la desintegració de l’urani. En el 1913, Kasimir Fajans i O.H. Göhring reclassificaren l’urani X i en distingiren, entre d’altres fraccions, l’urani X1.
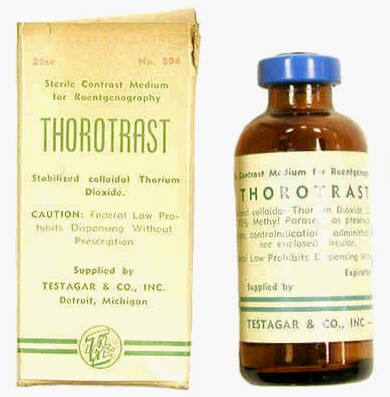
El “Thorotrast” fou un agent de contrast emprat en radiografia mèdica. Fou introduït en el 1931, amb diferents indicacions diagnòstiques. El principi actiu era el diòxid de tori. El tori ofereix una elevada absorció de raigs X i així permetia evidenciar estructures que serien invisibles en radiografies sense contrast. Els efectes secundaris immediats eren inferiors a la d’altres alternatives, per bé que ja en l’època algunes veus mostraren preocupació pels efectes a llarg termini. La semivida biològic de l’òxid de tori és de 22 anys, la qual cosa implicava una exposició continuada a alfa-radiació, especialment en el fetge, melsa, nodes limfàtics i ossos. En els anys 1950 caigué en desús. En total, es calcula que 2-10 milions de persones van ser rebre dosis de “Thorotrast”, amb una reducció en l’esperança de vida estimada en 14 anys, degut a l’augment del risc de desenvolupar càncer hepàtic i leucèmies.
Els avenços en la radioquímica i en el coneixement de la natura de la radioactivitats, fets en bona mesura amb compostos de tori, van ajudar a aclarir aquest garbuix. El pes atòmic calculat per al tori, 232, es corresponia únicament al pes atòmic de l’isòtop més present a la natura, el tori-232 (232Th). El radioactini de Hahn es corresponia al tori-227; el radiotori era tori-228; l’ioni de Boltwood era tori-230; l’urani Y d’Antonoff era tori-231; l’urani X<sub<1 era tori-234. De manera similar, el tori-A era poloni-216; el tori-B, plom-212; el tori-C, bismut-212; el tori-C’, poloni-212; el tori-C’’, tal•li-208 i el tori-D, plom-208. Finalment, el mesotori-1 era radi-228 i el mesotori-2 actini-228. El toró fou reclassificat com a radó-220 i el tori-X com a radi-224.
Sèrie de desintegració del tori. Consisteix en la cadena de desintegracions 4n que parteix del tori-232 i que conclou en el plom-208
Durant la Segona Guerra Mundial, l’aviació nord-americana emprà lents Aero-Lektar en màquines fotogràfiques de reconeixement. Alguns vidres d’aquestes lents contenien com a additiu òxid de tori, assolint concentracions de 11-13% de tori. L’òxid de tori permetia augmentar l’índex refractiu sense que pugés la dispersió. Amb el temps, algunes lents han adquirit una coloració de te, atribuïble a la radioactivitat del tori, encara que per autoradiografia siguin nivells pràcticament indetectables.

Lents fotogràfiques que contenen vidre amb òxid de tori com a additiu tendeixen a esgrogueir-se quan se les guarda durant força temps a la foscor (esquerra). Hom pot revertir aquest esgrogueïment si s’exposa la lent a radiació ultraviolada
En el 1945, Glen T. Seaborg mostrà que el tori havia de classificar-se en la taula periòdica com un actínid, concretament com el segon de la sèrie, i no pas en el grup IVa del titani, zirconi i hafni.
El reactor AVR, en funcionament entre el 1967 i 1988, fou un dels primers reactors nuclears que utilitzava el cicle del tori. Aquest cicle es basa en l’ús de tori-232 com a materials fèrtil. En el reactor, el tori-232 es transmuta en urani-233, que fa de material físsil. Els defensors de centrals nuclears de tori recorden la major abundància del tori en relació amb l’urani, la menor producció de plutoni i, per tant, el menor risc que les centrals nuclears siguin utilitzades per a proliferació d’armes nuclears.
El caràcter radioactiu del tori va fer qüestionar-ne algunes aplicacions. En el 1981, un estudi va estimar que la dosi resultant d’emprar una manta de tori cada cap de setmana durant un anys seria de 0,3-0,6 mrem, valor relativament petit en relació a l’exposició general normal de la població. Fins i tot, la ingesta d’una manta de tori típica (per a llums portàtils, de gas o de petroli) suposaria una dosi de 200 mrem. Més preocupant, però, era l’exposició dels treballadors que fabriquen aquestes mantes, així com la contaminació de sòls en emplaçaments propers a aquests fàbriques.
El tori: isòtops i abundància
Com a massa atòmica estàndard del tori hom pren la de 232,0377 uma, és a dir la corresponent a l’únic isòtop naturalment rellevant, el tori-232. Un llistat complet d’isòtops fa:
– tori-209 (209Th; 209,01772 uma). Nucli format per 90 protons i 119 neutrons. És un isòtop molt inestable, amb una semivida de 0,007 s.
– tori-210 (210Th; 210,015075 uma). És un isòtop molt inestable, amb una semivida de 0,017 s. Decau normalment a radi-206 (amb emissió d’un nucli d’heli-4) o, rarament, a actini-210 (amb emissió d’un positró).
– tori-211 (211Th; 211,01493 uma). Nucli format per 90 protons i 121 neutrons. És un isòtop molt inestable, amb una semivida de 0,048 s. Decau normalment a radi-207 (amb emissió d’un nucli d’heli-4) o, rarament, a actini-211 (amb emissió d’un positró).
– tori-212 (212Th; 212,01298 uma). Nucli format per 90 protons i 122 neutrons. És un isòtop molt inestable, amb una semivida de 0,036 s. Decau normalment (99,7%) a radi-208 (amb emissió d’un nucli d’heli-4) o, alternativament (0,3%), a actini-212 (amb emissió d’un positró).
– tori-213 (213Th; 213,01301 uma). Nucli format per 90 protons i 123 neutrons. És un isòtop molt inestable, amb una semivida de 0,14 s. Decau normalment a radi-209 (amb emissió d’un nucli d’heli-4) o, rarament, a actini-213 (amb emissió d’un positró).
– tori-214 (214Th; 214,011500 uma). Nucli format per 90 protons i 124 neutrons. És un isòtop molt inestable, amb una semivida de 0,1 s. Decau a radi-210 (amb emissió d’un nucli d’heli-4).
– tori-215 (215Th; 215,011730 uma). Nucli format per 90 protons i 125 neutrons. És un isòtop inestable, amb una semivida de 1,2 s. Decau a radi-211, amb emissió d’un nucli d’heli-4.
– tori-216 (216Th; 216,011062 uma). Nucli format per 90 protons i 126 neutrons. És un isòtop molt inestable, amb una semivida de 0,0268 s. Decau normalment (99,99%) a radi-212 (amb emissió d’un nucli d’heli-4) o, alternativament (0,006%), a actini-216 (amb emissió d’un positró). Posseeix dos estats mestastables, un a 2042 keV (216m1Th; que té una semivida de 1,37•10-4 s) i un altre a 2637 keV (216m2Th; que té una semivida de 6,15•10-7 s).
– tori-217 (217Th; 217,013114 uma). Nucli format per 90 protons i 127 neutrons. És un isòtop molt inestable, amb una semivida de 2,4•10-4 s. Decau a radi-213, amb emissió d’un nucli d’heli-4.
– tori-218 (218Th; 218,013284 uma). Nucli format per 90 protons i 128 neutrons. És un isòtop molt inestable, amb una semivida de 1,09•10-7 s. Decau a radi-214, amb emissió d’un nucli d’heli-4.
– tori-219 (219Th; 219,01554 uma). Nucli format per 90 protons i 129 neutrons. És un isòtop molt inestable, amb una semivida de 1,05•10-6 s. Decau a radi-215 (amb emissió d’un nucli d’heli-4) o, alternativament (0,0000001%), a actini-219 (amb emissió d’un positró).
– tori-220 (220Th; 220,015748 uma). Nucli format per 90 protons i 130 neutrons. És un isòtop molt inestable, amb una semivida de 9,7•10-6 s. Decau normalment a radi-216 (amb emissió d’un nucli d’heli-4) o, alternativament (0,0000002%), a actini-220 (per captura electrònica).
– tori-221 (221Th; 221,018184 uma). Nucli format per 90 protons i 131 neutrons. És un isòtop molt inestable, amb una semivida de 0,00173 s. Decau a radi-217, amb emissió d’un nucli d’heli-4.
– tori-222 (222Th; 222,018468 uma). Nucli format per 90 protons i 132 neutrons. És un isòtop molt inestable, amb una semivida de 0,002237 s. Decau normalment a radi-218 (amb emissió d’un nucli d’heli-4) o, alternativament (0,000000013%), a actini-222 (per captura electrònica).
– tori-223 (223Th; 223,020811 uma). Nucli format per 90 protons i 133 neutrons. És un isòtop molt inestable, amb una semivida de 0,6 s. Decau a radi-219, amb emissió d’un nucli d’heli-4.
– tori-224 (224Th; 224,021467 uma). Nucli format per 90 protons i 134 neutrons. És un isòtop inestable, amb una semivida de 1,05 s. Decau normalment a radi-220 (amb emissió d’un nucli d’heli-4) o, rarament, a radi-224 (amb emissió de dos positrons).
– tori-225 (225Th; 225,023951 uma). Nucli format per 90 protons i 135 neutrons. És un isòtop inestable, amb una semivida de 523 s (9 minuts). Decau majoritàriament (90%) a radi-221 (amb emissió d’un nucli d’heli-4) o, alternativament (10%), a actini-225 (per captura electrònica).
– tori-226 (226Th; 226,024903 uma). Nucli format per 90 protons i 136 neutrons. És un isòtop inestable, amb una semivida de 1834 s (31 minuts). Decau a radi-222, amb emissió d’un nucli d’heli-4.
– tori-227 (227Th; 227,0277041 uma). Nucli format per 90 protons i 137 neutrons. És un isòtop inestable, amb una semivida de 1,614•106 s (19 dies). Decau a radi-223, amb emissió d’un nucli d’heli-4. És present a la natura en forma de traça com a producte intermediari de la desintegració d’urani-235. Fou descrit originàriament per Otto Hahn en 1906 com a radioactini (RdAc).
– tori-228 (228Th; 228,0287411 uma). Nucli format per 90 protons i 138 neutrons. És un isòtop inestable, amb una semivida de 6,0326•107 s (2 anys). Decau normalment a radi-224 (amb emissió d’un nucli d’heli-4) o, alternativament (0,000000000013%), a plom-208 (amb emissió d’un nucli d’oxigen-20). És present a la natura en forma de traça com a producte intermediari de la desintegració de tori-232 (concretament, és isòtop fill de l’urani-232). Fou descrit originàriament per Otto Hahn el 1905 com a radiotori (RdTh; alternativament, tori-3).
– tori-229 (229Th; 229,031762 uma). Nucli format per 90 protons i 139 neutrons. És un isòtop inestable, amb una semivida de 2,316•1011 s (7340 anys). Decau a radi-225, amb emissió d’un nucli d’heli-4. Posseeix un estat metastable (229mTh) a 0,0076 keV, que té una semivida de 2,5•105 s i que decau a l’estat basal. Producte intermediari de la cadena de desintegració del neptuni-237, el tori-229 és isòtop fill de l’urani-233, i és present a la natura en forma de traça (associat a reactors nuclears naturals o artificials). És utilitzat com a precursor de l’actini-225 i del bismut-213, que tenen aplicacions en radiomedicina. La baixa energia d’excitació de 229mTh ha fet que se l’hagi proposat en diversos dispositius: emmagatzematge d’alta densitat d’energia, cronometria o computació quàntica.
– tori-230 (230Th; 230,0331338 uma). Nucli format per 90 protons i 140 neutrons. És un isòtop inestable, amb una semivida de 2,379•1012 s (75380 anys). Decau normalment a radi-226 (amb emissió d’un nucli d’heli-4) o, alternativament, a mercuri-206 (0,000000000056%; amb emissió d’un nucli de neó-24), o bé pot patir un procés de fissió espontània (0,00000000005%; amb diversos productes de fissió). És present a la natura en forma de traça, com a producte intermediari de la desintegració d’urani-238. Fou descrit originàriament per Bertram B. Boltwood, en el 1908, amb el nom de ioni (Io). És emprat en la tècnica de datació d’urani-tori o urani-ioni. Aquesta tècnica calcula l’edat de materials carbonacis (carbonats càlcics com coral, espeleotemes, etc.) d’acord amb el grau de recuperació de l’equilibri secular entre el tori-230 i el seu isòtop parental, l’urani-234. El tori-230 també és utilitzat en protocols s determinacions del flux de corrents oceànics.
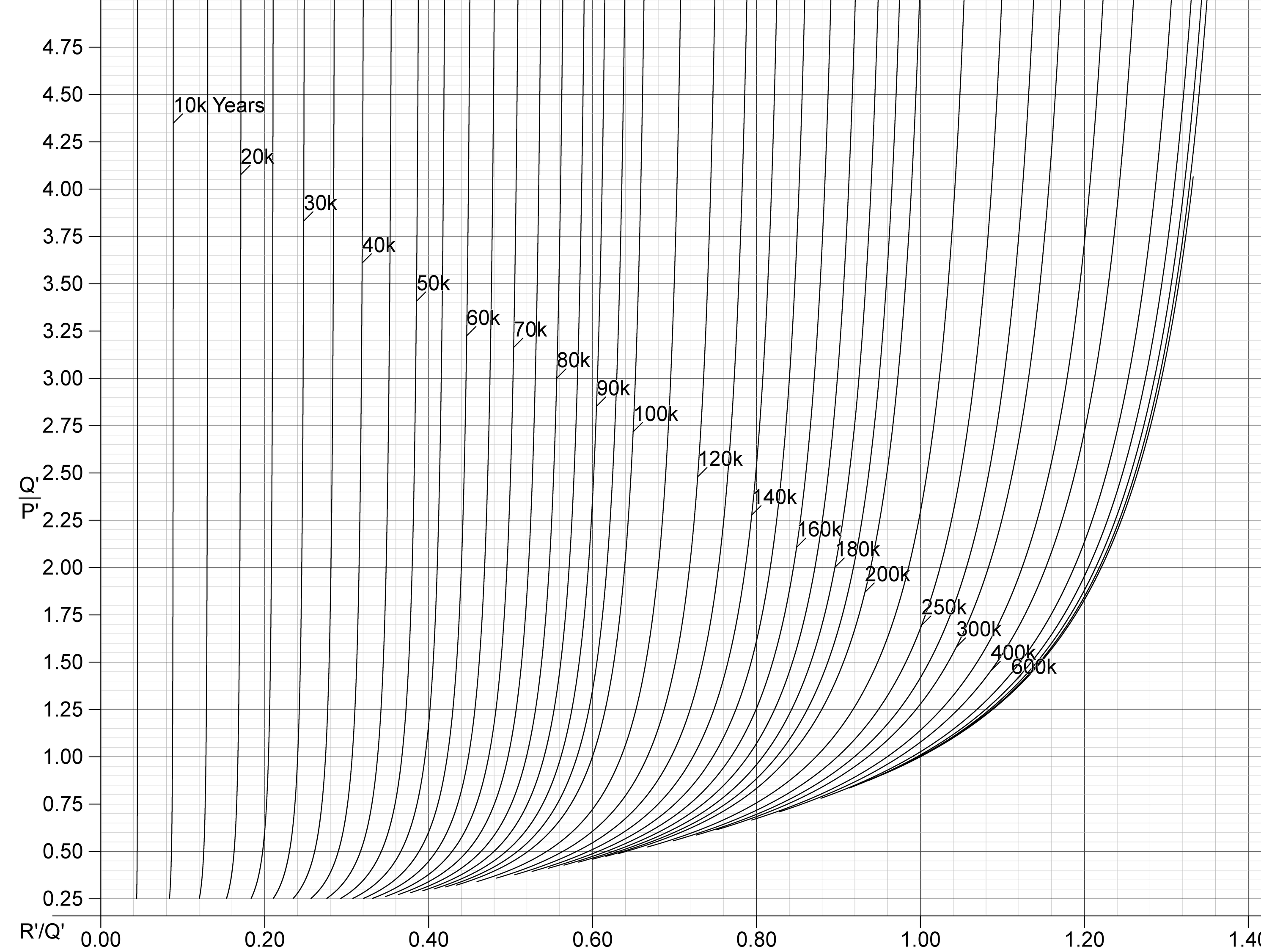
Relació entre 234U/238U (Q’/P’) i 230Th/234U, emprada en la datació urani-ioni. La tècnica val per a materials de menys de 500.000 anys d’antiguitat. Fa l’assumpció que el tori-230 de la mostra s’origina exclusivament a partir d’urani-234
– tori-231 (231Th; 231,0363043 uma). Nucli format per 90 protons i 141 neutrons. És un isòtop inestable, amb una semivida de 9,187•104 s (26 hores). Decau normalment a protactini-227 (amb emissió d’un electró) o, alternativament (0,00000001%), a radi-227 (amb emissió d’un nucli d’heli-4). És present a la natura en forma de traça, com a producte intermediari de la desintegració d’urani-235. Fou descrit originàriament per Antonoff en 1911 com a urani-Y (U-Y).
– tori-232 (232Th; 232,0380553 uma). Nucli format per 90 protons i 142 neutrons. És un isòtop inestable, amb una semivida de 4,434•1017 s (14000 milions d’anys). Decau normalment a radi-228 (amb emissió d’un nucli d’heli-4) o, rarament, a urani-232 (amb emissió de dos electrons) o a iterbi-182 (0,000000000278%; amb emissió d’un nucli de neó-26 i un altre de neó-24). També pot patir fissió espontània (0,0000000011%; amb diversos tipus de nuclis fills). És el tori per antonomàsia, en tant que l’únic isòtop de tori primordial a la Terra i pràcticament l’únic existent en mostres naturals.
– tori-233 (233Th; 233,0415818 uma). Nucli format per 90 protons i 143 neutrons. És un isòtop inestable, amb una semivida de 1310 s (22 minuts). Decau a protactini-233, amb emissió d’un electró.
– tori-234 (234Th; 234,043601 uma). Nucli format per 90 protons i 144 neutrons. És un isòtop inestable, amb una semivida de 2,08•106 s (24 dies). Decau a 234mPa, amb emissió d’un electró. És present a la natura en forma de traça, com a producte intermediari de la desintegració d’urani-238. Fou descrit originàriament per Fajans & Göhring en 1913 com a urani-X1 (U-X1).
– tori-235 (235Th; 235,04751 uma). Nucli format per 90 protons i 145 neutrons. És un isòtop inestable, amb una semivida de 430 s (7 minuts). Decau a protactini-235, amb emissió d’un electró.
– tori-236 (236Th; 236,04987 uma). Nucli format per 90 protons i 146 neutrons. És un isòtop inestable, amb una semivida de 2250 s (38 minuts). Decau a protactini-236, amb emissió d’un electró.
– tori-237 (237Th; 237,05389 uma). Nucli format per 90 protons i 147 neutrons. És un isòtop inestable, amb una semivida de 290 s (5 minuts). Decau a protactini-237 (amb emissió d’un positró).
– tori-238 (238Th; 238,0565 uma). Nucli format per 90 protons i 148 neutrons. És un isòtop inestable, amb una semivida de 560 s (9 minuts). Decau a protactini-238, amb emissió d’un electró.
L’àtom neutre de tori conté 90 electrons, amb una configuració basal d’escorça de 1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p66d27s2. Segons aquesta configuració, el podríem considerar com l’element del setè període del grup 4 (bloc d). No obstant, normalment se’l compta com un actínid, en el bloc f (de vegades en el grup f2, el grup del ceri). Pel que fa als comportaments tèrmics i elèctrics, el tori, com els altres primers actínids, als metalls de post-transició. És comptat entre els metalls naturals radioactius. L’estat d’oxidació més habitual és +4 (Th4+; amb cessió dels quatre electrons de 7s i 6d), encara que també el podem trobar amb +3 (Th3+; amb cessió de tres electrons de 7s i 6d, i el pas d’un electró de 6d a 5f), +2 (Th2+; amb cessió de dos electrons de 7s, i el pas d’un electró de 6d a 5f), +1 (Th+; amb cessió d’un dels electrons de 7s) i 0 (en el qual, en un estat d’excitació, un electró pot passar de 6d a 5f). El radi atòmic és de 1,798•10-10 m.

Làmina fina de tori metàl•lic de 0,1 grams de massa encapsulada en una ampolla de vidre en atmosfera d’argó
En condicions estàndards de pressió i de temperatura, el tori elemental es presenta com un sòlid metàl•lic d’aspecte argentí. És un metall tou (3,0 en l’escala de Mohs), molt dúctil i treballable. La densitat teòrica del tori pur en condicions estàndards és de 11724 kg•m-3 (entre els actínids, tan sols l’actini és encara menys dens). Entre els al•lòtrops sòlids hi ha:
– alfa-tori (α-Th): és al•lòtrop estable en condicions estàndards. Segueix una simetria cúbica centrada en les cares. En condicions estàndards de pressió, transiciona a beta-tori a 1720 K. Esdevé superconductor a temperatures inferiors a 1,4 K
– beta-tori (β-Th): segueix una estructura cristal•lina cúbica centrada en el cos.
– tori d’alta pressió: hi transiciona a altes pressions (102 GPa). Segueix una estructura tetragonal centrada en el cos.
En condicions estàndards de pressió, el tori (β-Th) fon a 2023 K i bull a 5061 K. Són els punts de fusió i ebullició més elevats de tots els actínids.
La puresa màxima assolida en la preparació de tori metàl•lic és de l’ordre del 99,9%, i la principal impuresa sol ser ThO2. En general, el tori és altament reactiu (amb oxigen, hidrogen, nitrogen, halògens, sofre). En condicions estàndards és poc atacable amb aigua, però sí és soluble en la majoria d’àcids (n’és excepció l’àcid clorhídric). El tori elemental en pols és pirofòric. Virolles de tori escalfades entren en ignició espontània, i produeixen una llum blanca fins que s’oxiden completament. Exposat a l’aire s’oxida en qüestió de mesos, adquirint primer una coloració grisa i després una pàtina negra.
En solucions aquoses, domina l’espècie Th4+, hidratada en [Th(H2O)9]4+: és el catió més gros dels actínids tetrapositius.
El tori pot formar aliatges amb molts metalls. Forma barreges eutèctiques amb el crom i l’urani. És completament miscible amb el ceri tan en estat sòlid com líquid.
Entre els compostos de tori podem esmentar:
– òxid de tori (ThO2). La tòria és un material refractari, amb el punt de fusió més elevat de tots els òxids coneguts (3663 K). Dewberry et al. (2007) aconseguiren la síntesi de ThO, que és la molècula més polar coneguda.
– hidròxid de tori (Th(OH)4).
– hidrurs: ThH2, Th4H15 (bon electroconductor).
– halurs: ThF4 (sòlid blanc, de 6300 kg•m-3), ThCl4 (sòlid blanc, de 4590 kg•m-3), ThBr4, ThI4, ThI3, ThI2.
– sulfurs: ThS (sòlid metàl•lic llustrós), Th2S3 (sòlid metàl•lic bru), Th7S12 (sòlid de color negre), ThS2 (sòlid de color porpre-bru), Th2S5 (sòlide calor taronja bru).
– seleniürs.
– tel•luriürs.
– nitrurs: ThN (sòlid de color groc daurat), Th3N4 (de color de bronze), Th2N3
– fosfurs: Th3P4, Th2P11, ThP7.
– arseniürs: Th3As4, ThAs2.
– antimoniürs: Th3Sb4, ThSb2.
– bismuturs: ThBi2.
– borurs: ThB6, ThB4, ThB12.
– carburs: ThC2 (sòlid refractari), Th2C3, ThC (sòlid refractari).
– compostots organotòrics: torocè (Th(C8H8)2; de color groc).
– aminodiboronat de tori: el tori hi presenta un nombre de coordinació de quinze. Aquest i altres compostos mostren que el tori és l’àtom que pot establir simultàniament més enllaços amb altres àtoms.
L’abundància atòmica del tori en l’univers és condicionada pels processos de nucleosíntesi en supernoves i per l’estabilitat dels seus isòtops. El tori-232 té una semivida un xic superior a l’edat actual de l’univers, la qual cosa condiciona favorablement la presència de tori. De fet, el tori-232 és el més estable de tots els isòtops d’elements transbismútics. Comptat i debatut, el tori és més abundant en termes atòmics que una sèrie d’elements més lleugers (tecneci, prometi, tuli, luteci, tàntal, poloni, àstat, radó, franci, radi i actini). Dels elements més pesants, no n’hi ha cap que superi el tori en abundància.
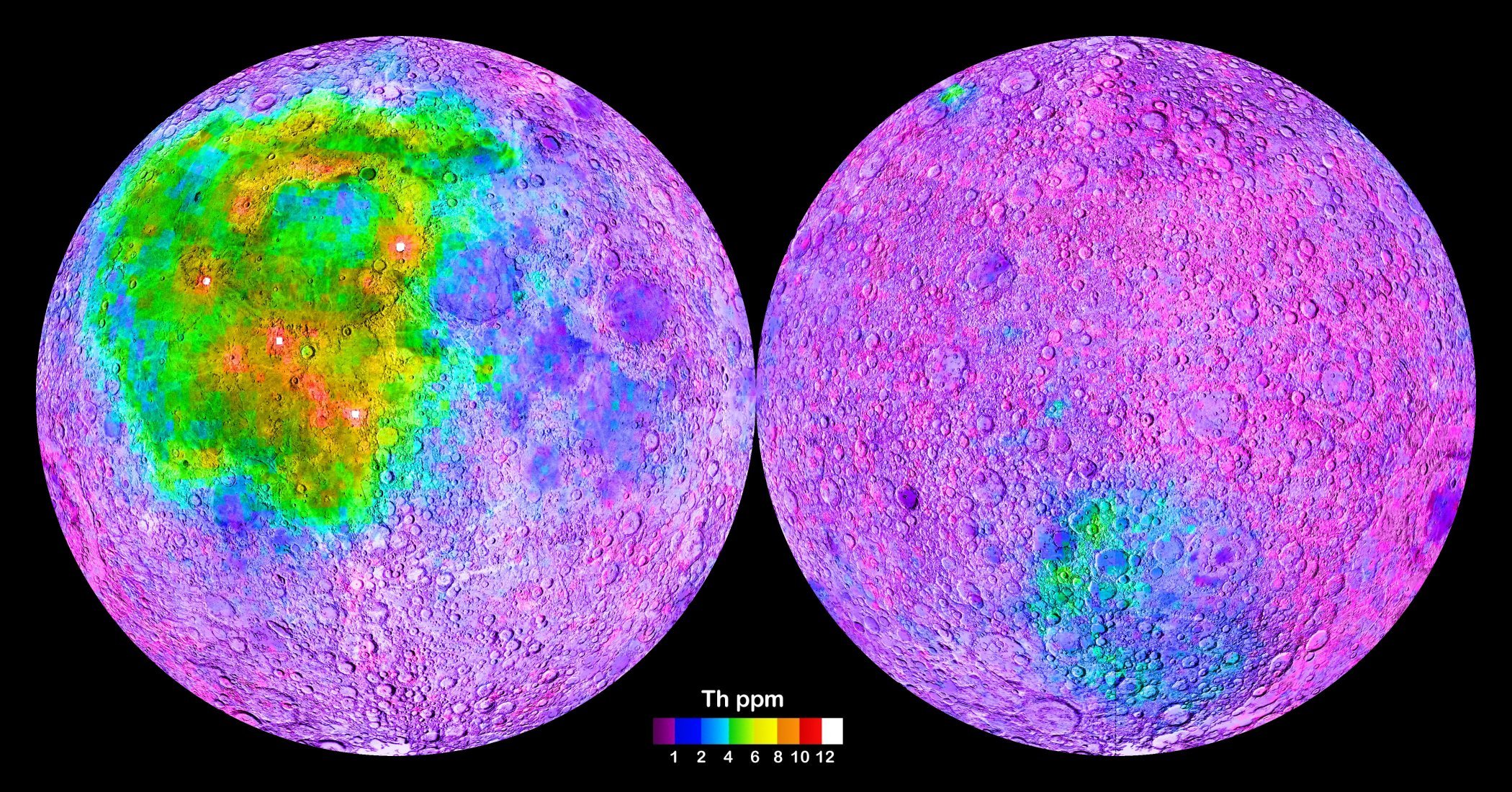
L’instrument de gammaespectroscopia de la Lunar Prospector va permetre cartografiar l’abundància de tori en la superfície lunar, car bona part de les emissions gamma són degudes a la radioactivitat del tori-232. En l’hemisferi subterrestre de la Lluna trobem la formació KREEP, que hauria tingut un enriquiment en potassi, elements de terres rares i fòsfor, degut possiblement a l’oceà de magma de la Lluna primigènia. En l’hemisferi antiterrestre trobem l’Anomalia Compton-Belkovich, que s’atribueix a una regió de vulcanisme intens fa 3-4 milers de milions d’anys. Mapes similars al de la imatge s’han obtingut de la Terra i de Mart
En la Terra, globalment, l’abundància de tori és de 0,06 ppm en termes de massa (0,006 ppm en termes atòmics). L’únic isòtop primordial és el tori-232 (pràcticament el 100% de freqüència isotòpica), per bé que també trobem altres cinc isòtops en quantitats menors: tori-230, tori-231, tori-228, tori-227, tori-234. El tori-232 i l’urani-238 són actualment els isòtops més importants en la generació de calor interna en el planeta Terra.
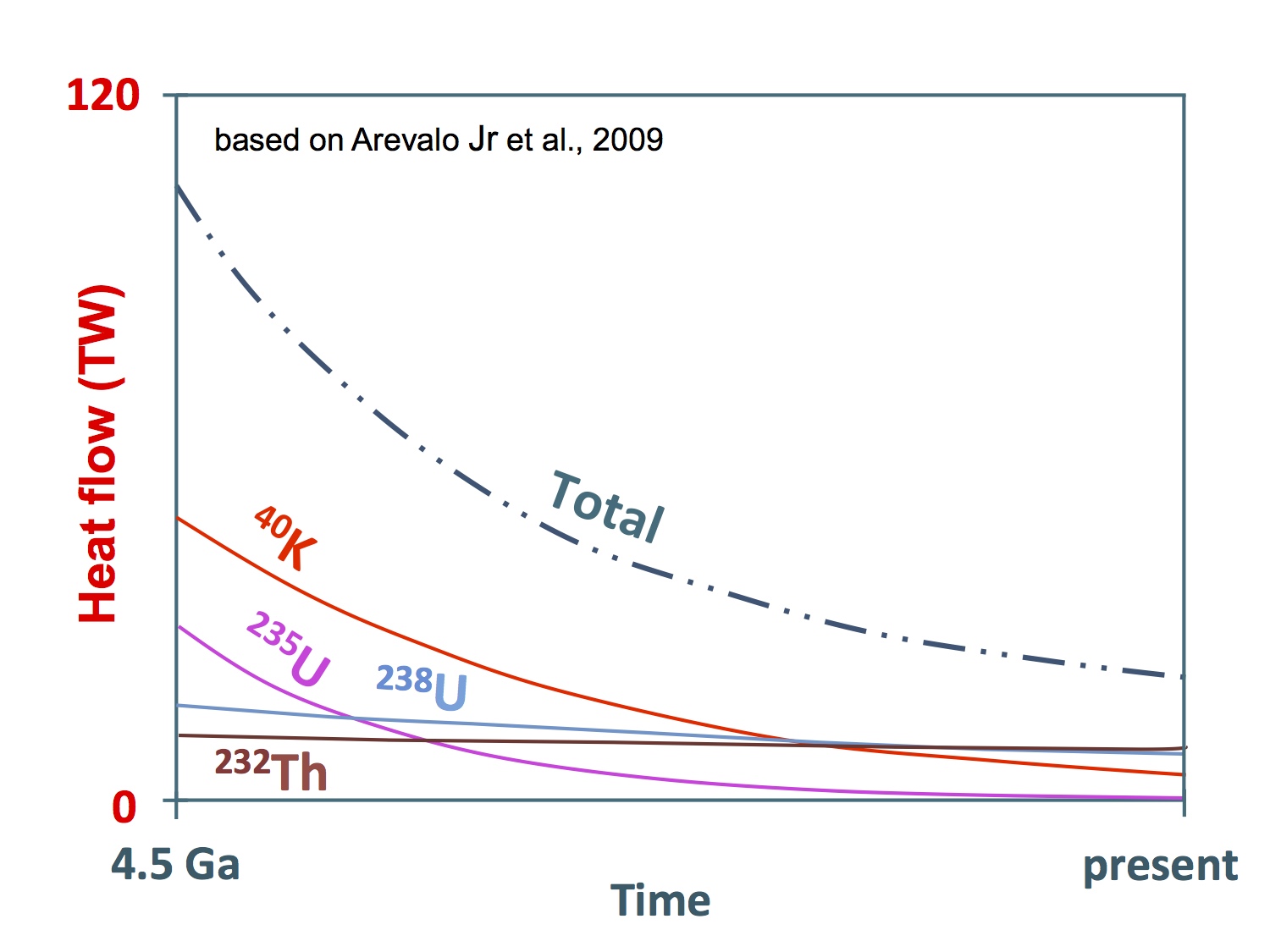
La generació interna de calor de la Terra depèn del contingut primordial de radioisòtops i, molt particularment, de potassi-40, urani-235, urani-238 i tori-232. A mesura que s’esgoten, la generació interna de calor disminueix. En els darrers centenars de milions d’anys, el tori-232 i l’urani-238 són els principals contribuents (Arevalo et al., 2008).
En l’escorça terrestre, l’abundància del tori és de 9 ppm en termes de massa (amb una variació geogràfica de 0,8-13,5 ppm). El minerals més ric en tori són la torianita (12% d’òxid de tori), la torita (ThSiO4) o la torianita (ThO2 + UO2). Més comuna és la monazita (amb un contingut del 2,5% del tori). Altres minerals amb concentracions notables de tori són l’al•lanita (0,1-2%) o alguns zirconis (fins a un 0,4%). En minerals sense presència d’urani, el tori-232 és pràcticament l’únic isòtop present (el segon més abundant és 228Th, amb una ratio 228Th:232Th de <10-10). En minerals d’urani, encara que el tori-232 continua a dominar, també s’hi troben traces de 234Th i 230Th (productes de l’urani-238) i 231Th i 227Th (productes de l’urani-235), i en algun cas la freqüència isotòpica del 230Th pot arribar al 25%. La radioactivitat del tori produeix en els minerals que el contenen metamictització (destrucció parcial de l’estructura cristal•lina degut a l’emissió de nuclis d’heli-4). El tori el trobem fonamentalment en forma combinada, amb un estat d’oxidació de +4. El contingut típic de tori en sòls de 6 ppm, per bé que amb fortes variacions d’acord amb el context geològic.
En termes generals, els compostos de tori són poc solubles en aigua. La concentració típica en oceans és de 1 μg•m-3. En les aigües abissals, la freqüència isotòpica de tori-230 passa a ser, encara que petita, significativa.
En l’atmosfera, el tori és present de manera transitòria en forma de traça.
El tori no és, pel que se sap, bioelement per a cap organisme. És present a la biosfera de manera passiva.
En un cos humà adult de 70 kg, podem trobar típicament uns 100 μg de tori. La ingesta típica diària és de 3 μg de tori. Aquesta exposició és més elevada en personal que treballa o viu a prop de mines d’urani, estany o fosfat (o en dipòsits rics en tori en general), així com en les indústries que processen aquests materials o en cementiris nuclears. Del tori ingerit, tan sols s’absorbeix el 0,02%. Del tori absorbit, un 75% s’acumula en l’esquelet.
El tori metàl•lic, a més de radioactiu, és pirofòric. De totes formes, les quantitats de tori que poden haver, per exemple, en una manta incandescent, no obliguen a prendre cap mesura específica contra la radiació. De totes formes, cal tenir present l’impacte radiològic dels productes de desintegració del tori-232, particularment de radi-228 i del radó-220. L’exposició laboral a aerosols rics en tori s’ha demostrat com a factor de risc en l’adquisició de càncer de pulmó i pàncrees i neoplàsies hemàtiques.
Aplicacions del tori
La principal font industrial de tori és la monazita, que conté difosfat de tori (Th(PO4)2). La monazita pot ser tractada amb àcid nítric, de la qual cosa en resulta nitrat de tori, que és tractat amb tributil-fosfat. També pot ser tractada amb una solució aquosa de NaOH 45% a 410 K, i els hidròxids metàl•lics resultants són rentats i concentrats amb àcid clorhídric: la neutralització a pH = 5,8 permet la precipitació diferencial de Th(OH)4. En tots dos casos, són necessaris procediments per eliminar les impureses, que consisteixen sobretot en terres rares.

Sorra de monazita
El tori metàl•lic es prepara a partir de ThO2, per exemple, fent-lo reaccionar amb calci en una atmosfera inert, per un procés d’electròlisi (a partir de ThCl4) o per un procés de cristal•lització en barra (a partir de ThI4)
Hom calcula les reserves accessibles de tori en 1.900.000 tones, concentrades a Índia (litoral de Bengala) i Austràlia. La quantitat global en l’escorça seria de 120 bilions de tones.
Ja hem vist com les primeres aplicacions industrials del tori són anteriors a la descoberta de la seva radioactivitat. El caràcter radioactiu del tori ha animat, en general, a trobar substituts en les aplicacions.
Una aplicació no-radioactiva que resisteix és la soldadura de gas inert (argó o heli) i tungstè. El tori s’utilitza com a recoberta dels fils de tungstè per millorar-ne l’emissió d’electrons. El contingut de tori pot ser de l’1% (EWTH-1) o del 2% (EWTH-2).
També resulta difícil substituir l’òxid de tori en mantes incandescents, ja que l’òxid d’itri i altres terres rares són menys eficients i més cares.
El diòxid de tori s’utilitza en vidre per augmentar l’índex refractiu i disminuir la dispersió, per exemple en la confecció de lents d’alta qualitat en fotografia o en instrumental científic. El tetrafluorur de tori s’empra encara com a material antireflectant en revestiments òptics, ja que amb capes superiors d’altres materials queda minimitzada la radiació alfa procedent del tori.
Més desplaçat es troba l’òxid de tori en la confecció de ceràmiques termoresistents, encara que s’utilitza en la confecció de gresols de laboratori. També ha caigut en desús el seu ús com a catalitzador (en la conversió d’amoníac en àcid nítric).
El tori-229 és emprat en medicina nuclear, com a precursor de l’actini-225 i, sobretot, del bismut-213, utilitzats per exemple en el desenvolupament de radiofàrmacs antitumorals.
Les freqüències isotòpiques del tori participen en dos mètodes radiomètrics de datació:
– el mètode d’urani-tori es fonamenta en la desintegració d’urani-234 en tori-230. És referit sovint a la desintegració d’urani-235 en tori-231/protactini-231. Com que els compostos de tori i de protactini no són tan solubles com els d’urani en aigua, aquest mètode és utilitza en la datació de sediments oceànics, particularment de carbonat càlcic.
– el mètode d’ioni-tori es fonamenta en la ratio 232Th:230Th. Com més antic és el sediment, més elevada hauria de ser aquesta ratio, de manera que hom pot datar mostres de fins a 400.000 anys d’antiguitat. Això és útil en la determinació de les taxes oceàniques de sedimentació.
L’aplicació amb més potencial del tori és, doncs, l’ús en centrals nuclears. El tori-229 és un isòtop fissible, amb una massa crítica estimada en 2839 kg, però que amb reflectors d’acer podria davallar a 994 kg. No obstant, més aviat es pensa en l’ús del tori-232 com a “material fèrtil” en tant que en un reactor nuclear transmutaria, per captura de neutró, a urani-233, que és un isòtop fissible.
En una central nuclear de tori, doncs, el material fissible és l’urani-233. La generació de neutrons continuada de neutrons permet sostindre la generació d’urani-233 a partir de tori-232. Hom cita com a avantatges d’aquestes centrals nuclears la major abundància del tori en l’escorça terrestre, la major seguretat en el nucli del reactor (major estabilitat química, punt de fusió superior, etc.), la menor generació de residus transurànics (plutoni, etc.).
Ara bé, les centrals de tori, amb la tecnologia actual, no van més enllà de la fase experimental. Per iniciar el funcionament, cal irradiar amb neutrons grans quantitats de tori-232. L’Agència de l’Energia Nuclear ha considerat que les centrals comercials de tori no seran viables fins que hom no depassi el “pic de l’urani”, és a dir quan el mineral d’urani assoleixi preus prohibitius.