Fil conductor d’aquesta sèrie és el concepte de descoberta científica, de l’ampliació de coneixements. La nit del 13 de març del 1781, William Herschel observa el cel a través del telescopi instal•lat en el seu jardí del nombre 19 de New King Street, en Bath (Somerset). Herschel, natural de Hannover, fill d’una família musical i músic ell mateix, s’havia endinsat plenament en la dedicació astronòmica i en la construcció de telescopis no feia ni vuit anys, a l’edat de 35, empès per la seva amistat amb l’Astrònom Reial, Nevil Maskelyne. En aquelles nits, Herschel feia observacions sistemàtiques d’estels, per calcular-ne la posició al llarg de l’any, per tal de cercar una mesura de la paral•laxi a partir de la qual estimar científicament la distància a la qual es troben. Encara que s’hi havia fet alguns intents en aquest sentit, Herschel no donava cap per bo, i ni ell mateix, en els 40 anys de vida que li quedaven, hi reeixiria. En qualsevol cas, aquella nit va anotar que “en el quartil proper a ζ Tauri” hi havia un objecte remarcable que “o és un estel nebulós o un cometa”. La nit del 17 de març observà la mateixa zona del cel, i trobà que l’objecte s’havia desplaçat en relació de ζ Tauri i dels altres estels, de manera que descartà que fos un “estel nebulós”. Havia d’ésser, doncs, un cometa. Així es publicà el 26 d’abril a la Royal Society. En aquest report, Herschel oferia de diàmetre aparent de l’objecte i de la trajectòria seguida. Ja abans de presentar la comunicació, Herschel l’havia notificat a Maskelyne. Maskelyne mateix hi va fer les seves observacions i, el 23 d’abril, escrivia a Herschel per dir-li “que no sé com anomenar-lo; és tan probable que sigui un planeta regular que es mou en una òrbita gairebé circular al sol com un cometa que es mogués en una el•lipsi molt excèntrica; no n’he vist cap cabellera ni cua”. Johann Elert Bode ja assenyalava que es podria tractar “d’un objecte planetoidal fins ara desconegut que circulés més enllà de l’òrbita de Saturn”. En el 1783, Anders Johan Lexell calculava l’òrbita de l’objecte, que era gairebé circular, com la d’un planeta, i no pas gaire excèntrica. Herschel, llavors, ja podia concloure que es tractava “d’un planeta primari del nostre Sistema Solar”. Els altres planetes primaris eren coneguts des de l’Antiguitat i, descomptant la Terra, havien rebut els noms de divinitats, Mercuri, Venus, Mart, Júpiter i Saturn. Herschel considerà que el nom que se li havia de donar s’havia de correspondre a la contemporaneïtat i així el denomina “Georgium Sidus” o “Planeta Georgià”, en honor al rei Jordi III d’Anglaterra. Jérôme Lalande havia proposat que se li donés senzillament el nom del seu descobridor, “Herschel”. Erik Prosperin suggerí el nom de Neptú, per mantenir la tradició de denominar el planeta amb els noms de déus, tota vegada que així alhora s’homenatjava la Potència Naval de Gran Bretanya (un nom de compromís podia ser Neptú Jordi III o Neptú Britània). Bode, de manera similar, havia proposat el nom d’Urà, en la idea d’una gradació de planetes exteriors generacional: “Mart, fill de Júpiter, fill de Saturn, fill d’Urà”. Sivry proposà un altre nom diví, però de dea, Cíbele. La controvèrsia terminològica continuà uns anys. Alhora, també hi havia una qüestió. El planeta de Herschel és un planeta de magnitud aparent de 5-6, és a dir que entra en el camp de visió a ull nu. Abans de Herschel, però, qui l’havia observat l’havia tractat com un estel. Aquest fou el cas de Pierre Lemonnier que, entre 1750 i 1769, anotà l’objecte com si fossin estels diferents i diverses posicions. John Flamsteed l’observà en sis ocasions en 1690, però el catalogà com si fos un estel fix (34 Tauri). És possible que en el catàleg d’Hiparc, Urà aparegués també com un estel fix. Però això no li treu la descoberta real de Herschel. Herschel sempre defensà el nom de “Georgium Sidus”, però el nom d’Urà semblava més respectuós i menys carregat políticament. L’Almanac Nàutic de Sa Majestat mantingué el nom de “Georgium Sidus” fins el 1850, quan el substituí per “Uranus”, que ja havia esdevingut el nom d’acceptació general.

El planeta Urà observat pel Telescopi Hubble en el 2005. El planeta Urà fou descobert per Herschel en 1783, qui també en descobrí els dos primers satèl•lits en 1787. En el 1789, Herschel descrigué un possible anell planetari, encara que la descoberta definitiva dels anells d’Urà va haver d’esperar el 10 de març del 1977, quan el Kuiper Airborne Observatory estudià l’ocultació de l’estel SAO 158687 per Urà. En el 24 de gener del 1986, Voyager 2 realizà una aproximació de 81.500 km de la superfície (gasosa) d’Urà. Aquesta missió, l’única realitzada, juntament amb els telescopis orbitals dels nostres dies, han permès adquirir una idea de la dinàmica atmosfèrica d’aquest planeta
Martin Heinrich Klaproth i la descoberta de l’urani

Professor de química de l’Artilleria Reial Prussiana des de 1787, assessor farmacèutic del Col•legi Mèdic Superior des de 1782 i ell mateix propietari d’una farmàcia de Berlín, Klaproth, a 46 anys, ja és una de les figures més prestigioses en els cercles científics alemanys interessats en la química i la mineralogia. En el 1789 publicà una memòria a Chemische Annalen titulada “Chemische Untersuchung des Uranits, einer neuentdeckten metallischen Substanz”. En efecte, Klaproth havia analitzat mostres de pechblenda. En digerir-les en àcid nítric, i després neutralitzat la solució amb sosa càustica, hom podia obtenir un precipitat de color groc. Aquest precipitat, escalfat amb carbó, es reduïa a una pols negra.

Espècimen de pechblenda
Klaproth, d’acord amb el paradigma de la química de Lavoisier, interpretà que la pols negra en qüestió era una substància metàl•lica, mentre que el precipitat de color groc en seria l’òxid corresponent. Klaproth proposà el noms d’urani (uranium) per al “nou metall”, el d’urània per a la terra o òxid groc i el d’uranita per designar el mineral. Amb el nom d’“uranium”, Klaproth volia homenatjar a William Herschel, descobridor vuit anys abans d’un “nou planeta”, i ho feia adoptant la denominació que Johann Elert Bode defensava per designar aquest astre.
La proposta fou generalment ben rebuda, i potser fins i tot va ajudar a fixar el nom d’Urà per designar el planeta trans-saturnià. Però es considerà que la separació elemental del nou metall no s’havia assolit, i que la pols negra descrita per Klaproth era més aviat un òxid que no pas un metall.
Pel que fa a la denominació d’uraninita per al mineral, penetrà més en uns països que en uns altres. El nom de pechblenda fou retingut. Aquest mot alemany significa literalment “quitrà lluent” i apareix ja documentat en el segle XV, per exemple com a un dels minerals explotats en les mines d’argent de Jáchymov (Bohèmia). Gairebé tota la producció de pechblenda provenia d’aquestes mines. Bona part del consum el feia a la mateixa Bohèmia la indústria del vidre, com a colorant groc. L’arqueologia ens ensenya que aquest ús ja s’havia aplicat en l’antiguitat. En efecte, en restes de Pompeia hom ha trobat l’ús d’òxid d’urani com a colorant groc en ceràmiques. I, en el 1912, R. T. Gunther reportà que vidre groc recuperat d’una vil•la romana del cap Pusilleco, a Nàpols tenia un contingut d’òxid d’urani de l’1%.

Vidre d’urani, sota el transil•luminador. La radiació ultraviolada provoca una fluorescència verda degut al contingut d’òxid d’urani (típicament, del 2%)
En el 1808, a “New System of Chemical Philosophy”, John Dalton esmenta l’urani en el llistat de 36 “elements simples”, i el simbolitza amb la lletra “U”. També és aquest símbol el que utilitza Berzelius en 1813. No obstant, altres autors utilitzaran el símbol “Ur”. El nom d’urani ha estat acceptat per totes les llengües, amb les modificacions oportunes. En txec hom intentà el nom de “nebesník” (“nebe” vol dir cel), però no aconseguí desplaçar el nom internacional d’“uran”.
En el 1841, Eugène-Melchior Péligot (1811-1890), professor de química analítica de l’Institut Nacional Agronòmic, aconseguí per primera vegada la purificació d’urani metàl•lic. En efecte, la substància groga aïllada per Klaproth no era òxid d’urani, sinó probablement diuranat sòdic; alhora, la substància negra resultant de reduir aquesta sal groga era realment òxid d’urani (UO2). Péligot dissolgué pechblenda en àcid clorhídric, obtenint clorur d’urani (UCl4) que després reduïa amb potassi metàl•lic. La purificació d’urani permetia aconseguir una sèrie de mesures directes de propietats fonamentals, com ara la del pes atòmic.
En el 1865, John Newlands classifica l’urani (U) en el sistema d’octaus, com l’element número 40 inclòs en el grup del bor.
No és gaire diferent del criteri que utilitzarà Mendeleev en el 1869: l’urani (Ur = 116) apareix en el cinquè període, adscrit al grup del bor.
Però aquest criteri Mendeleev el revisa. Noves dades de pes atòmic indiquen que l’urani és l’element més pesant de totes. Així, en la taula del 1871, l’urani (U = 240) apareix en la dotzena sèrie (setè període), en el grup de l’oxigen. En dècades posteriors, aquest grup serà separat en dos, i l’urani serà considerat com l’element del setè període del grup del crom, del molibdè i del tungstè.
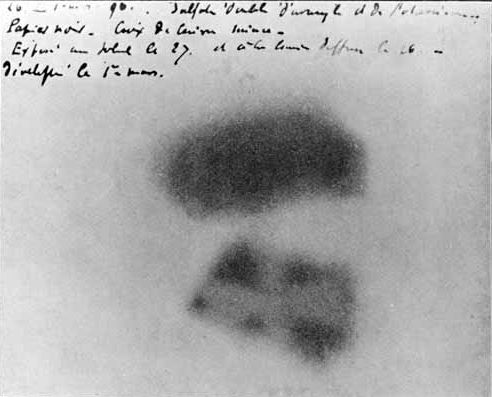
Autoradiografia obtinguda per Henri Becquerel de dos monticles de sal d’urani. En el de sota hi ha interposada una creu de malta metàl•lica
En el 1896, Henri Becquerel descrigué que l’uranilsulfat potàssic (K2UO2(SO4)2) era capaç per si sol d’imprimir plaques fotogràfiques. Becquerel féu aquesta descoberta mentre investigava la fluorescència de la sal d’urani, però s’adonà que es tractava d’una propietat diferent. Aquests “raigs d’urani” foren coneguts ràpidament com a “raigs de Becquerel”. Com ja havia passat l’any anterior amb els “raigs de Röntgen”, diversos investigadors s’interessaren en els aspectes teòrics i pràctics del fenomen. El matrimoni Curie adquirí tones de pechblenda, i a través d’anàlisis químiques descrigueren dos elements encara més radioactius que l’urani, el poloni i el radi. Alhora, hom també descrivia la radioactivitat del tori.
En el 1900, William Crookes descrivia en mostres d’urani una substància química desconeguda, solible en hidròxid d’amoni i en carbonat d’amoni, a la que denominà provisionament “urani X”. En el 1902, Frederick Soddy i Ernest Rutherford descrivien les transmutacions químiques que duien de l’urani al plom. Hans Geiger & Ernest Rutherford (1910) diferenciaren entre l’urani 1 i l’urani 2 que, encara que químicament idèntics, ocupaven diferents llocs en aquesta cadena de transmutacions. En el 1913, Fajans & Göhring diferenciaven entre l’urani X1 i l’urani X2, bo i assignant el primer a l’element 91. El mateix any, Soddy proposava ja una “llei de desplaçaments” per a les transmutacions radioactives. La radioquímica contribuïa així a dotar d’entitat física els conceptes de nombre atòmic i de massa atòmica. En el 1917, Hahn descrivia l’urani Y i l’urani Z. Així hom ja podia elaborar una seqüència de transmutacions:
U 1 → U X1 → U X2 → U Z → U 2 → U Y
L’urani 1 es corresponia a l’urani-238, mentre l’urani 2 era l’urani-234. L’urani X2 i l’urani Z eren dos formes del protactini-234. L’urani X1 era tori-234 i l’urani Y era tori-231.
La producció de radi amb diferents finalitats exigia el processament de grans quantitats de mineral d’urani. Això va esperonar un creixement de les aplicacions d’urani en la indústria del vidre i de la ceràmica, però també en el sector tèxtil (sals d’urani com a mordants de seda o de llana), en el cuir (com a pigments), etc. El nitrat d’urani fou emprat en tinta seca per a reprografia.

Oscar D’Agostino, Emilio Segré, Edoardo Amaldi, Franco Rasetti i Enrico Fermi, retratats en el pati de l’Institut de Física de la Universitat de Roma, a la Via Panisperna
En el 1934, el grup d’Enrico Fermi a Roma observà que el bombardament d’urani amb neutrons produïda radiacions beta. Hom pensà que els productes d’aquest bombardament eren els elements immediatament transurànics, l’element 93 i l’element 94, i el degà de la Facultat, Orso Mario Corbino s’afanyà a denominar-los “ausoni” i “hesperi”, en un doble homenatge a Itàlia. Però això fou descartat eventualment en pro d’una conclusió encara més espectacular: els nois de la Via Panisperna havien aconseguit la fissió d’urani.
Sobre la fissió d’urani, havien treballat Otto Hahn i Frist Strassmann a Berlin, i el febrer del 1939, Lise Meitner i Otto Robert Frisch encunyaven ja l’expressió “fissió nuclear”, alhora que explicaven les bases atòmiques del procés. Fermi, ja als Estats Units, hipotetitzà que la producció de neutrons per la fissió nuclear d’urani podia fer sostingut el procés.
En el 1935, Arthur Dempster havia descrit l’actino-urani, que resulta ser un nou isòtop de l’urani, l’urani-235. En el 1939, Fermi calculà que per a l’urani-235, per cada fissió s’emetien de mitjans uns 2,5 neutrons. Així doncs, l’urani-235 era realment un material fissible per neutrons termals. L’urani-238, en canvi, no era un material fissible directament. Ara bé, en el 1940, McMillan & H. Abelson aconseguiren la síntesi per primera vegada d’element 93 per irradiació d’urani amb neutrons, alhora que Seaborg et al. aconseguien poc després la síntesi d’element 94 per irradiació d’urani amb deuterons. L’element 93 i l’element 94 reberen els noms, respectivament, de neptuni i de plutoni, en correspondència amb els planetes transuranians. La transmutació de l’urani-238 a plutoni donava lloc a un material físsil.
Leó Szilárd ja havia concebut la idea de reaccions nuclears en cadena en 1933 i, juntament amb Enrico Fermi, patentà la primera proposta de reactor nuclear. L’energia nuclear de fissió no tan sols tenia finalitats civils, sinó que podia ser aprofitada bèl•licament. A final del 1939, ja esclatada la guerra, Szilárd i Einstein escrigueren a Franklin D. Roosevelt sobre la possibilitat d’armes nuclears. Paral•lelament, a Alemanya, s’havia format una Uranverein.
Dels diferents projectes el que aniria més lluny seria el nord-americà (Projecte Manhattan). El 2 de desembre del 1942, un equip liderat per Enrico Fermi iniciava, amb Chicago Pile-1, la primera reacció nuclear en cadena autosostinguda. Com a matèries primeres havien emprat 360 tones mètriques de grafit, 53 d’òxid d’urani i 5,5 d’urani metàl•lic, procedents majoritàriament de la Westinghouse Lamp Plant.

Peces d’urani metàl•lic obtingudes en el decurs del projecte Manhattan
El Projecte Manhattan fou coronat amb dos tipus de bombes atòmiques. Un era una bomba d’urani, que emprava com a material físsil urani altament enriquit en 235U (80%). L’altre era una bomba de plutoni, que emprava com a material físsil plutoni sintetitzat a partir d’urani-238. El 16 de juliol del 1945 es va fer esclatar Alamogordo, Nou Mèxic una bomba de plutoni, Trinity. La guerra ja havia acabat a Europa, de manera que les autoritats militars alemanys havien tingut raó en 1942 quan pensaven que les armes nuclears no decidirien la guerra. Però el Japó resistia en la lluita contra els Estats Units, i el 6 d’agost del 1945, la primera bomba d’urani era llençada contra la ciutat d’Hiroshima.

Núvol nuclear deixat damunt d’Hiroshima per Little Boy, la bomba nuclear d’urani-235, que havia deixat anar el Boeing B-29 Enola Gay, comandat pel coronel Paul W. Tibbets, Jr. La bomba contenia 64 kg d’urani enriquit (80% de 235U), del qual es calcula que menys d’1 kg va entrar en fissió nuclear com a conseqüència de la detonació, a 580 metres per damunt de la ciutat. La potència explosiva, de totes manera, fou equivalent a 12500 tones de TNT. L’explosió i l’ona tèrmica provocaren directament la mort de 75.000 persones i la destrucció de 50.000 edificis. La destrucció fou total en un radi de 1,6 km, i s’hi produïren incendis en una superfície total de 11 km2.
En el 1946, Glenn T. Seaborg parlà de l’urani-233 com d’un isòtop físsil addicional a l’urani-235 i al plutoni-239. L’urani-233 es podria sintetitzar a partir de la irradiació amb neutrons de tori-232. En les dècades següents, els Estats Units produïren en els reactors de Hanford i de Savannah River un total de 2 tones d’urani-233, amb un cost de l’ordre de 2-4 milions de dòlars/kg. L’urani-233 entrà en la formulació de diverses armes nuclears a partir del 1955.
També es deu a Seaborg, per aquesta època, la consolidació definitiva de l’urani i del tori, i de la resta d’actínids en el bloc f de la taula periòdica.
El 20 de desembre del 1951, el Experimental Breeder Reactor I, de l’Argonne National Laboratory, situat a Arco (Idaho) fou el primer reactor nuclear en produir energia elèctrica.

Quatre bombetes de 150 W il•luminades el Nadal del 1951 per energia nuclear al Reactor d’Arco, Idaho
El 27 de juny del 1954 entrava en funcionament el reactor AM-1 d’Obninsk (Kaluga), la primera central nuclear connectada a la xarxa com a productora neta. El primer submarí de propulsió nuclear fou, també el 1954, el USS Nautilus.
El desenvolupament d’armes nuclears i les consegüents proves atòmiques, així com l’extensió de l’energia nuclear per a usos civils comportà un augment de la demanda d’urani. Els minerals d’urani no resultaren tan rars com inicialment s’havia previst. Però les bombes nuclears d’Hiroshima i de Nagasaki, juntament amb l’amenaça permanent d’una guerra mundial nuclear d’efectes devastadors, canviaren la percepció de la radioactivitat. En gairebé totes les aplicacions industrials, hom cercà substituts no-radioactius als compostos d’urani.
Tall geològic de la localitat d’Oklo (Gabon). Damunt del granit (4) hi ha gres (2) solcat per una capa de mineral d’urani, en la qual s’hi troben zones corresponents a reactors nuclears naturals. Ja en 1956, Paul Kazuo Kuroda (1917-2001) havia predit l’existència de reactors nuclears de fissió d’origen natural en dipòsits prou rics d’urani. En el 1972, Francis Perrin (1901-1992) en va descobrir indicis a Oklo, d’acord amb les distribucions isotòpics de neodimi i ruteni. És l’únic cas conegut a la Terra, i es tracta d’un complex de 16 localitzacions que haurien acollir reaccions autosostingudes de fissió nuclear fa 1700 milions d’anys. Les reaccions es van perllongar durant centenars de milers d’anys generant 100 kW. En aquella època, la freqüència isotòpica de l’urani-235 encara era del 3,1%, de manera que la interacció del dipòsit ric en urani i les aigües subterrànies permeté aquest procés, que es considera impossible en les condicions naturals actuals
En el 2007, es va viure una bombolla en el preu d’urani, que passà de valors de 20$/kg (2005) a 300$/kg. Un motor d’aquesta pujada fou la incertesa quant a la producció de mines com la de Cigar Lake (Saskatchewan), però també hi ajudà la idea que els programes de centrals nuclears d’Índia i Xina dispararien la demanda. La pujada animà la inversió de prospeccions i l’interès per aprofitar el contingut d’urani dels oceans. Però quan els preus d’urani passaren en mesos a 100$/kg, hom retornà a una certa normalitat.
Evolució del nombre de caps nuclears armamentístics de les dues principals potències nuclears, Estats Units i Rússia. El Tractat de No Proliferació d’armes nuclears també considera potències nuclears a Xina, França, Regne Unit i Estats Units. Cal tindre present també que Índia, Pakistan i Corea del Nord també tenen armes nuclears.
L’urani: isòtops i abundància
La massa atòmica estàndard de l’urani és de 238,02891 uma, que resulta de la mitjana ponderada dels seus isòtops naturals (238U, 235U, 234U). Un llistat complet dels isòtops coneguts fa:
– urani-217 (217U; 217,02437 uma). Nucli format per 92 protons i 125 neutrons. És un isòtop molt inestable, amb una semivida de 0,026 s.
– urani-218 (218U; 218,02354 uma). Nucli format per 92 protons i 126 neutrons. És un isòtop molt inestable, amb una semivida de 0,006 s. Decau a tori-214, amb emissió d’un nucli d’heli-4.
– urani-219 (219U; 219,02492 uma). Nucli format per 92 protons i 127 neutrons. És un isòtop molt inestable, amb una semivida de 0,055 s. Decau a tori-215, amb emissió d’un nucli d’heli-4.
– urani-220 (220U; 220,02472 uma). Nucli format per 92 protons i 128 neutrons. És un isòtop molt inestable, amb una semivida de 6•10-8 s. Decau normalment a tori-216 (amb emissió d’un nucli d’heli-4) o, rarament, a protactini-220 (amb emissió d’un positró).
– urani-221 (221U; 221,02640 uma). Nucli format per 92 protons i 129 neutrons. És un isòtop molt inestable, amb una semivida de 7•10-7 s. Decau normalment a tori-217 (amb emissió d’un nucli d’heli-4), o rarament, a protactini-221 (amb emissió d’un positró).
– urani-222 (222U; 222,02609 uma). Nucli format per 92 protons i 130 neutrons. És un isòtop molt inestable, amb una semivida de 1,4•10-6 s. Decau normalment a tori-218 (amb emissió d’un nucli d’heli-4) o, alternativament (0,000001%), a protactini-222 (amb emissió d’un positró).
– urani-223 (223U; 223,02774 uma). Nucli format per 92 protons i 131 neutrons. És un isòtop molt inestable, amb una semivida de 2,1•10-5 s. Decau a tori-219, amb emissió d’un nucli d’heli-4.
– urani-224 (224U; 224,027605 uma). Nucli format per 92 protons i 132 neutrons. És un isòtop molt inestable, amb una semivida de 9,4•10-4 s. Decau a tori-220, amb emissió d’un nucli d’heli-4.
– urani-225 (225U; 225,02939 uma). Nucli format per 92 protons i 133 neutrons. És un isòtop molt inestable, amb una semivida de 0,061 s. Decau a tori-221, amb emissió d’un nucli d’heli-4.
– urani-226 (226U; 226,029339 uma). Nucli format per 92 protons i 134 neutrons. És un isòtop molt inestable, amb una semivida de 0,269 s. Decau a tori-222, amb emissió d’un nucli d’heli-4.
– urani-227 (227U; 227,031156 uma). Nucli format per 92 protons i 135 neutrons. És un isòtop inestable, amb una semivida de 66 s. Decau normalment a tori-223 (amb emissió d’un nucli d’heli-4) o, alternativament (0,001%), a protactini-227 (amb emissió d’un positró).
– urani-228 (228U; 228,031374 uma). Nucli format per 92 protons i 136 neutrons. És un isòtop inestable, amb una semivida de 550 s (9 minuts). Decau normalment (95%) a tori-224 (amb emissió d’un nucli d’heli-4) o, alternativament (5%), a protactini-228 (per captura electrònica).
– urani-229 (229U; 229,033506 uma). Nucli format per 92 protons i 137 neutrons. És un isòtop inestable, amb una semivida de 3500 s (58 minuts). Decau majoritàriament (80%) a protactini-229 (amb emissió d’un positró) o, alternativament (20%), a tori-225 (amb emissió d’un nucli d’heli-4).
– urani-230 (230U; 230,033940 uma). Nucli format per 92 protons i 138 neutrons. És un isòtop inestable, amb una semivida de 1,80•106 s (21 dies). Decau normalment a tori-226 (amb emissió d’un nucli d’heli-4) o, alternativament, a tori-230 (rarament, amb emissió de dos positrons) o bé pateix fissió espontània (0,00000000014%; amb diversos productes resultants).
– urani-231 (231U; 231,036294 uma). Nucli format per 92 protons i 139 neutrons. És un isòtop inestable, amb una semivida de 3,6•105 s (4 dies). Decau normalment a protactini-231 (per captura electrònica) o, alternativament (0,004%), a tori-227 (amb emissió d’un nucli d’heli-4).
– urani-232 (232U; 232,0371562 uma). Nucli format per 92 protons i 140 neutrons. És un isòtop inestable, amb una semivida de 2,17•109 s (69 anys). Decau normalment a tori-228 (amb emissió d’un nucli d’heli-4) o, alternativament, a plom-208 (0,00000000089%; amb emissió d’un nucli de neó-24), a mercuri-204 (0,000000000005%; amb emissió d’un nucli de magnesi-28) o pateix fissió espontània (0,000000000001%; amb generació de diversos productes). És present a natura en forma de traça, en tant que subproducte indesitjat de reactors nuclears.
– urani-233 (233U; 233,0396352 uma). Nucli format per 92 protons i 141 neutrons. És un isòtop inestable, amb una semivida de 5,024•1012 s (159.200 anys). Decau normalment a tori-229 (amb emissió d’un nucli d’heli-4) o, alternativament, a plom-209 (0,000000000072%; amb emissió d’un nucli de neó-24) o a mercuri-205 (0,00000000000013%; amb emissió d’un nucli de magnesi-28) o bé entra en fissió espontània (0,000000006%; amb generació de diversos productes). L’urani-233 és sintetitzat a partir de tori-232 amb irradiació de neutrons, i ha estat utilitzat com a material físsil en reactors nuclears experimentals. En la Terra primigènia els nivells eren més elevats, en tant que producte intermediari de la desintegració del neptuni-237.
– urani-234 (234U; 234,0409521 uma). Nucli format per 92 protons i 142 neutrons. És un isòtop inestable, amb una semivida de 7,716•1012 s (245.500 anys). Decau normalment a tori-230 (amb emissió d’un nucli d’heli-4) o, alternativament, a mercuri-206 (0,000000000014%; amb emissió d’un nucli de magnesi-28) o a hafni-184 (0,000000000009%; amb emissió d’un nucli de neó-26 i un altre de neó-24) o bé pateix fissió espontània (0,00000000173%; amb generació de diversos productes). La freqüència isotòpica és de 0,0054%, amb oscil•lacions mostrals de 0,005-0,0059%. És producte intermedi de la desintegració de l’urani-238. Fou descrit originàriament en 1910 per Hans Geiger i Ernest Rutheford com a “urani II” (o urani 2, simbolitzat U II). L’urani-234 és emprat en sistemes de datació, com l’urani-tori o l’urani-urani. En aquest darrer sistema, la ratio 234U/238U és aplicable a la datació de materials de 10.000 a 2 milions d’anys d’antiguitat. L’urani-234 posseeix un estat metastable a 1421,32 keV (234mU), que té una semivida de 0,0335 s.
– l’urani-235 (235U; 235,0439299 uma). Nucli format per 92 protons i 143 neutrons. És un isòtop inestable, amb una semivida de 2,22•1016 s (704 milions d’anys). Decau normalment a tori-231 (amb emissió d’un nucli d’heli-4) o, alternativament, a hafni-186 (0,0000000008%; amb emissió d’un nucli de neó-25 i un altre de neó-24) o entra en fissió espontània (0,000000007%; amb generació de diversos productes). La freqüència isotòpica actual a la Terra és de 0,7204%, amb oscil•lacions mostrals de 0,7198% a 0,7207%. A la Terra és bàsicament un isòtop primordial, si bé tan sols es conserva una petita fracció de l’urani-235 originari (la freqüència isotòpica inicial rondaria el 20%). Fou descobert originàriament per Arthur Jeffrey Dempster per espectrometria de masses; Dempster el denominà actino-urani (Ac U) i poc temps després fou identificar com l’isòtop 235 de l’urani. Mitjançant diversos mètodes (difusió, centrifugació, etc.), hom pot arribar a enriquiments isòtopics d’urani-235 del 90%, si bé per a les aplicacions de reactors nuclears n’hi ha prou a arribar al 3-4%. Com a contrapartida, en resulta un urani empobrit (amb freqüències de 235U inferiors al 0,3%). La ratio 207Pb/235U és una de les emprades en el mètode de datació urani-plom. L’urani-235 posseeix un estat metastable (235mU) a 0,0765 keV, que té una semivida de 1600 s, i que decau a l’estat basal.
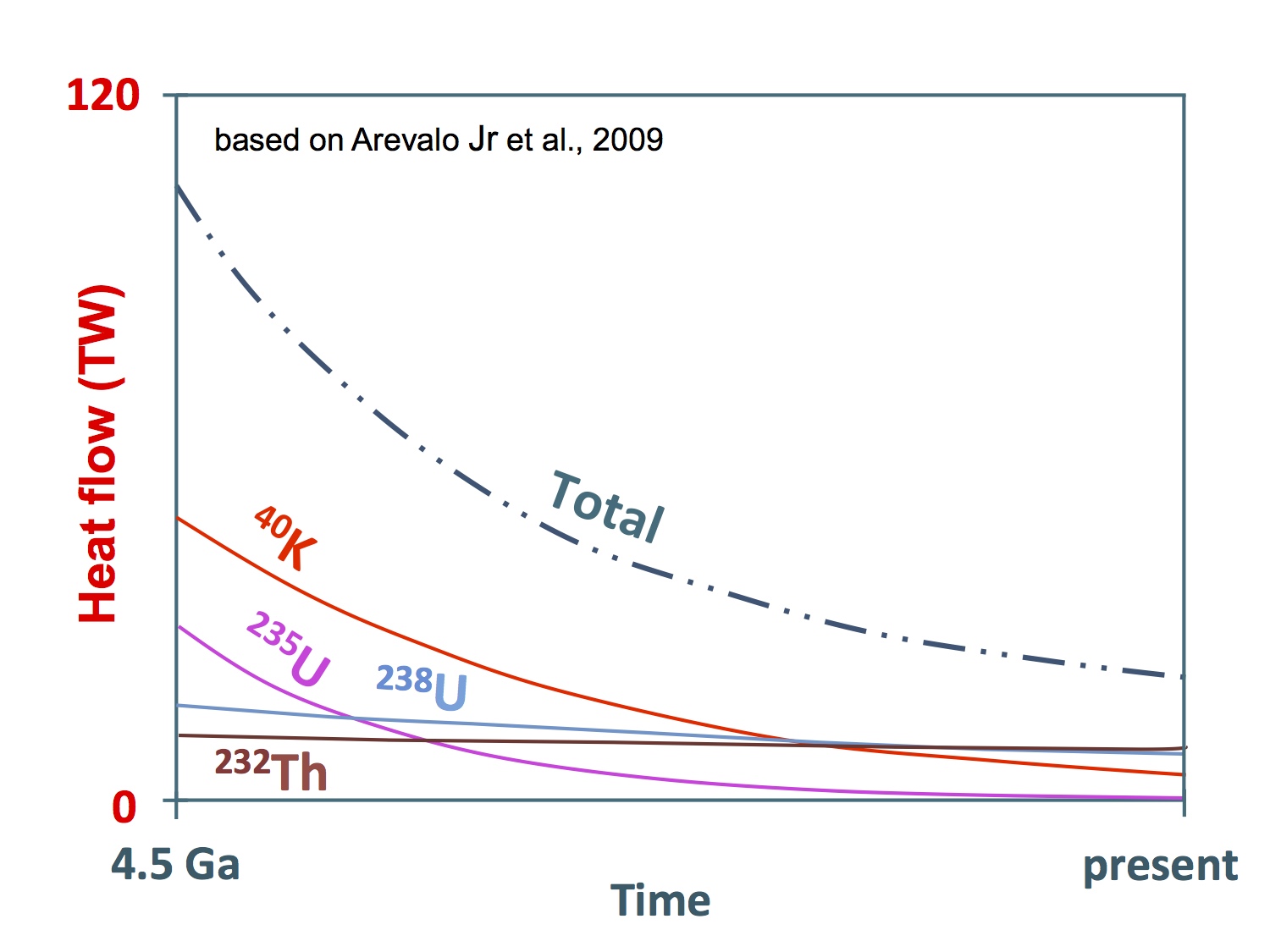
La calor radiogènica de la Terra primigènia era produïda particularment pel potassi-40 i l’urani-235. L’exhauriment de les dotacions primordials d’aquests radioisòtops han suposat una caiguda continuada del flux energètic.
– urani-236 (236U; 236,045568 uma). Nucli format per 92 protons i 144 neutrons. És un isòtop inestable, amb una semivida de 7,391•1014 s (23 milions d’anys). Decau a tori-232 (amb emissió d’un nucli d’heli-4) o, alternativament, entra en fissió espontània (0,000000096%; amb generació de diversos productes). Posseeix dos estats metastables, un a 1052,89 keV (236m1U; que té una semivida de 1•10-7 s) i un altre a 2750 keV (236m2U; que té una semivida de 1,2•10-7 s). L’urani-236 és produït en reactors nuclears, on el 18% dels àtoms d’urani-235 que absorbeixen un neutró termal generen urani-236 per comptes de fissionar-se, i és considerat com a part del residu nuclear de radioactivitat perllongada. És present a la natura en forma de traça, majoritàriament com a conseqüència dels assaigs de bombes nuclears en els anys 1950 i 1960. En la Terra primitiva, era generat com a producte intermediari de la desintegració del plutoni-244.
– urani-237 (237U; 237,0487302 uma). Nucli format per 92 protons i 145 neutrons. És un isòtop inestable, amb una semivida de 5,83•105 s (7 dies). Decau a neptuni-237, amb emissió d’un electró. És present a la natura en forma de traça, derivat de l’urani-238.
– urani-238 (238U; 238,0507882 uma). Nucli format per 92 protons i 146 neutrons. És un isòtop inestable, amb una semivida de 1,410•1017 s (4468 milions d’anys). Decau normalment a tori-234 (amb emissió d’un nucli d’heli-4) o, alternativament, a plutoni-238 (0,000000000219%; amb emissió de dos electrons) o entra en fissió espontània (0,0000545%; amb generació de diversos productes). La freqüència isotòpica és de 99,2742%, amb variacions mostrals de 99,2739%-99,2752%. Es conserva gairebé la meitat de la dotació primordial a la Terra. Fou descrit originàriament per Hans Geiger i Ernest Rutherford en 1910 com a urani I o urani 1 (U I). És utilitzat en sistemes de datació d’urani-urani i urani-plom. Encara que no és material físsil, se l’utilitza com a material fèrtil en reactors nuclears, ja que en capturar un neutró dóna lloc al plutoni-239. Així és doncs la matèria primera de reactors i bombes de plutoni. L’urani-238 posseeix un estat metastable (238mU) a 2557,9 keV, que té una semivida de 2,8•10-7 s.
– urani-239 (239U; 239,0542933 uma). Nucli format per 92 protons i 147 neutrons. És un isòtop inestable, amb una semivida de 1407 s (23 minuts). Decau a neptuni-239, amb emissió d’un electró. És present a la natura en forma de traça, format arran de la captura d’un neutró per part d’un nucli d’urani-238. L’urani-239 posseeix dos estats metastables, un a 20 keV (239m1U; que té una semivida de més de 2,5•10-7 s) i un altre a 133,799 keV (239m2U; que té una semivida de 7,8•10-7 s).
– urani-240 (240U; 240,056592 uma). Nucli format per 92 protons i 148 neutrons. És un isòtop inestable, amb una semivida de 5,08•104 s (14 hores). Decau normalment a neptuni-240 (amb emissió d’un electró) o, alternativament (0,0000000001%), a tori-236 (amb emissió d’un nucli d’heli-4). En la Terra primitiva, era generat com a producte intermediari de la desintegració del plutoni-244.
– urani-241 (241U; 241,06033 uma). Nucli format per 92 protons i 149 neutrons. És un isòtop inestable, amb una semivida de 300 s (5 minuts). Decau a neptuni-241, amb emissió d’un electró.
– urani-242 (242U; 242,06293 uma). Nucli format per 92 protons i 150 neutrons. És un isòtop inestable, amb una semivida de 1010 s (17 minuts). Decau a neptuni-242, amb emissió d’un electró.
L’àtom neutre d’urani conté 92 electrons, amb una configuració basal d’escorça de 1s22s22p63s23p63d104s24p64d104f145s25p65d105f36s26p66d17s2. És comptat entre els actínids, és a dir entre els elements del període 7 del bloc f. De vegades, se’l considera dins del grup f4, el lantànid del qual seria el neodimi. És classificat entre els metalls naturals radioactius. L’estat d’oxidació més habitual és +6, encara que també el trobem en +5, +4, +3, +2,. +1 i 0. El radi atòmic és de 1,56•10-10 m.

Barra d’urani empobrit, de 10 grams
En condicions estàndards de pressió i temperatura, l’urani elemental es presenta com un sòlid metàl•lic de color gris argentí. S’han descrit tres al•lòtrops:
– alfa-urani (α-U). És l’al•lòtrop estable fins a 930 K, amb una estructura cristal•lina ortoròmbica. És un material relativament dur (6 en l’escala de Mohs), mal•leable i dúctil, amb una densitat de 19100 kg•m-3. És un material paramagnètic i de certa resistivitat elèctrica (0,28 μΩ•m).
– beta-urani (β-U). És estable a temperatures de 930-1030 K. Segueix una estructura tetragonal.
– gamma-urani (γ-U). És estable a temperatures superiors a 1030 K.
En condicions estàndards de pressió, l’urani elemental (γ-U) fon a 1405,3 K. L’urani líquid té una densitat en el punt de fusió de 17300 kg•m-3.
En condicions estàndards de pressió, l’urani elemental bull a 4404 K.
La radioactivitat de l’urani natural es manifesta en l’emissió d’alfa-radiació, a la qual contribueix en un 49% l’urani-238, un 49% l’urani-234 i un 2% l’urani-235.
En contacte amb l’aire, l’urani metàl•lic desenvolupa una capa d’òxid, de color negre, que es desprèn fàcilment. En general, l’urani metàl•lic és força reactiu. És atacable amb àcid clorhídric i àcid nítric. La pols d’urani pot reaccionar fins i tot amb aigua freda.

Pols groga d’urani de baix enriquiment. La pols groga calcinada, producte del refinat d’urani consisteix en una barreja d’òxids d’urani
Entre els compostos d’urani podem esmentar:
– òxids: UO2 (sòlid de color negre, 10970 kg•m-3), UO3 (sòlid de color groc-taronja), U3O8, UO, U2O5, UO4•2 H2O.
– hidrur: UH3 (sòlid de 10950 kg•m-3).
– halurs: UF4 (sòlid de color verd, 6700 kg•m-3), UF3, UF6 (sòlid incolor, de 5090 kg•m-3), UCl4, UBr3, UBr4, UI3, UI4.
– oxihalurs: UO2F2, UOCl2, UO2Cl2, UO2Br2.
– carburs: UC, UC2, U2C3.
– nitrurs: UN, UN2, U2N3.

Color de solucions de sals d’urani amb diferents nombres d’oxidació
L’abundància atòmica de l’urani en l’univers és condicionada pels processos de nucleosíntesi en supernoves i per l’estabilitat dels seus isòtops, així com per les rutes de desintegració del neptuni i del plutoni. És sobretot l’estabilitat relativa de l’urani-238, la que fa que l’urani sigui relativament abundant pel lloc que ocupa en la taula periòdica. Així, l’urani supera en abundància atòmica un grapat d’elements més lleugers (tecneci, prometi, poloni, àstat, radó, franci, radi, actini i protactini). Cap dels elements transurànids assoleix una abundància mínimament comparable a la de l’urani.
En el planeta Terra, l’urani assoleix una abundància global de 0,02 ppm en termes de massa (0,002 ppm en termes atòmics). Com a element litòfil, l’urani és molt més concentrat en l’escorça, on arriba a 1,8 ppm en termes de massa. En sòls, la concentració pot oscil•lar de 0,7 a 11 ppm (amb valors de 15 ppm en sòls agrícola degut a l’ús de fosfats minerals, que poden ser relativament rics en urani). L’urani-238 del mantell terrestre és, juntament amb el tori-232 i el potassi-40, un dels principals responsables de la calor interna planetària, font d’energia responsable de la fluïdesa del nucli extern (alhora responsable de la generació del camp magnètic) i dels moviments de convecció del mantell (alhora responsable de la tectònica de plaques).
En l’escorça, l’urani es troba gairebé sempre de forma combinada, amb U3O8 com un dels composts més comuns. El contingut total d’urani en l’escorça terrestre és de l’ordre de 1017 kg. És present en un ample ventall de minerals, els més destacats dels quals són la uraninita o pechblenda, la carnotita, l’autunita, l’uranofà, la torbenita i la coffinita. Com hem dit els dipòsits de fosfats solen ser rics en urani, com també ho són els dipòsits de lignita o les sorres de monazita.
La presència d’urani en la hidrosfera depèn del context geològic. La concentració típica en l’oceà és de 0,003 ppm, la qual cosa suposa un contingut total d’urani en l’oceà de 1013 kg.
La presència d’urani en l’atmosfera és transitòria i en forma de traça.
L’urani no és, pel que se sap, bioelement per a cap organisme. És present a la biosfera de forma passiva, encara que alguns microorganismes són capaços de metabolitzar-lo. Així, bacteris com Shewanella putrefaciens o Geobacter metallireducens són capaços de reduir compostos d’urani (VI) en compostos d’urani (IV). Uns altres organismes són capaços d’acumular urani, i així Citrobacter és capaç d’assolir concentracions d’urani 300 vegades superior a la del medi exterior a través de l’absorció d’ions uranil (UO22+). També el liquen Trapelia involuta és capaç d’absorbir grans quantits d’urani, mentre que el fong Glomus intraradices facilita l’acumulació d’urani per part de la planta en les arrels de la qual viu. Aquests organismes poden ser interessants en bioremediació d’aigües o sòls contaminats amb urani.
La majoria de plantes absorbeixen urani del sòl, i poden assolir concentracions de 0,005-0,060 ppm per matèria seca (i de 4 ppm per cendres).
En el cos humà, la concentració típica d’urani és de 0,0013 ppm en termes de massa (30 ppb en termes atòmics). Així el contingut per a un pes corporal de 70 kg seria de 0,1 mg. La ingesta típica diària és de l’ordre de 1-2 μg d’urani. Les exposicions a urani i als seus isòtops fills radioactius (radi, radó, poloni, etc.) poden ser majors per a treballadors (p. ex., en plantes de processament de fosfats minerals; plantes de processament o enriquiment d’urani) i en entorns on es realitzen proves atòmiques o s’hi llençaren armes convencionals que incorporaven urani empobrit. De l’urani ingerit, tan sols s’absorbeix un 0,5-5%, sobretot en forma d’ió uranil. L’urani no s’absorbeixen pràcticament per via cutània, però la pols per via inhalada si pot perjudicar els pulmons. De l’urani absorbit, una bona part s’acumula en els ossos, amb una alta persistència.
Pel que fa a la toxicitat, l’urani, a més de radioactiu, és un metall pesant. Finament dividit, a més és pirofòric.

Peça d’urani altament enriquit. Fins i tot en aquests casos, l’urani metàl•lic pot ser manipulat amb els guants adequats. En pols, l’urani i els seus compostos són més perillosos, i cal garantir que no hi hagi exposicions per inhalació i ingesta
L’economia de l’urani
La producció mundial anual d’urani, expressada en pasta groga (>75% equivalent a U3O8) és de 70.000 tones anuals. N’ha mines d’urani a cel obert, subterrànies, explotacions de lixiviació in situ, perforacions, etc. Cal destacar la producció de l’Àsia Central, de Nord-amèrica, Austràlia, Níger i Namíbia. De caràcter experimental, són diversos projectes que volen recuperar urani de l’aigua marina.

Evolució de la producció minera d’urani i de la demanda des de la fi de la Segona Guerra Mundial. El preu d’urani pateix oscil•lacions degut a la irregularitat de la producció, cosa que ha estimulat les inversions en prospeccions mineres
Les reserves mundials econòmicament accessibles d’urani (
N’hi ha prou amb concentracions de 0,01% d’òxid d’urani en el mineral perquè pugui ser rendible l’extracció. A banda d’aquests minerals de baix contingut (0,01-0,25%), s’exploten minerals amb continguts més elevats (de fins a un 23% d’òxids d’urani). El mineral és esmicolat, i la pols resultant és lixiviada amb àcid o àlcali. Hi segueixen diverses rondes de precipitació, extracció amb solvents i bescanvi iònic. La pasta groga que en queda és calcinada i sotmesa a processos de refinament i conversió.
A banda de les fonts minerals, una entrada menor d’urani la constitueix el desmantellament d’armes nuclears.
L’urani metàl•lic de grau comercial és produït amb la reducció d’halurs d’urani amb metalls alcalins o alcalinoterris. Per a la producció d’urani molt pur, hom recorre a la descomposició termal d’halur en filament calent.
L’urani natural té una freqüència isotòpica d’urani-235 de 0,72%. Gràcies a processos d’enriquiment hom pot assolir freqüències isotòpiques del 90%. Hom calcula que hi ha unes reserves de 2000 tones d’urani altament enriquit. El més habitual és un enriquiment baix de 3-4%. Subproducte de l’enriquiment, és l’urani empobrit.

Central nuclear de Vandellòs. El reactor d’aigua pressuritzada de Vandellòs II continua operatiu després de 34 anys. Com a combustible emprat òxids d’urani enriquit (amb freqüència isotòpica d’urani-235 del 2-4%). Aquest tipus de reactors suposen el 60% de la producció elèctrica amb energia nuclear
La principal aplicació civil de l’urani és com a combustibles en centrals nuclears. Cada quilogram d’urani-235 produeix, comptant-ne la fissió completa, 20 TJ. Com a combustible, les centrals nuclears solen emprar urani enriquit fins al 2-4% d’urani-235. Alguns tipus de centrals (CANDU, Magnox) poden treballar amb urani no-enriquit.
Cal recordar també algunes aplicacions menors de l’urani i dels seus composts:
– l’acetat i el format d’uranil són utilitzats com a agents de contrast en microscòpia electrònica de transmissió.
– el metall d’urani és utilitzat en alguns aparells de raigs X d’alta energia.
– algunes relacions isotòpics d’urani són utilitzades en tècniques de datació.
Entre les aplicacions militars, cal esmentar l’ús d’urani empobrit en l’elaboració de munició d’alta penetració. L’urani empobrit és aliat amb 1-2% de titani, molibdè, etc. L’elevada densitat, duresa i piroforicitat d’aquest material el fa capaç de penetrar en objectius blindats (tancs, etc.).

Mapa de Kosovo que mostra les àrees que van rebre projectils de l’OTAN amb urani empobrit en 1999
L’ús d’aquestes municions per part d’Estats Units i de l’OTAN al sud d’Irac (1991), a Kosovo (1999) i a altres ha constituït un focus de contaminació d’urani de les regions afectades. Encara que l’urani empobrit és molt menys radioactiu que l’urani natural, sí conserva la toxicitat pròpia d’aquest metall pesant.
Les mesures contra la proliferació d’armes nuclears han reduït l’aplicació de l’urani en bombes nuclears. A més de l’ús d’urani-235 com a material físsil, l’urani-238 és el material fèrtil a partir del qual se sintetitza el plutoni-239.