La nostra visió mediterràneo-cèntrica ens fa qualificar la रसायन (rasayana, “essència del camí”) com “l’alquímia índia o hindú”, encara que l’enfocament de la रसशास्त्र (rasasatra, “essència del mercuri”) és sobretot mèdic. Certament, hi ha connexions entre les diferents escoles índies i les homòlogues que trobem en l’àrea persa i aràbiga, les quals connectaven amb les fondes tradicions egípcies, babilònies i gregues, i alhora amb les existents en el subcontinent europeu. L’analogia d’aquestes escoles ja la Abu Rayahn Biruni (segle XI e.c.), en vincular l’alquímia i la “rasayana”. Per Biruni, “rasa” volia dir “or”. Però si en l’alquímia de l’Afràsia occidental, el protagonisme el té l’or, sembla que en la “rasayana” la palma se la duia l’hidrargent o argentviu (el metall líquid identificat amb el planeta-déu Mercuri). La “rasayana” s’havia interessat especialment per la “rasasatra” a partir del segle VIII e.c. Nagarjuna (nascut a Gujarat en el 931 e.c.) ens ha deixat diversos tractats metal•lúrgics i químics, on s’expliquen els mètodes d’extracció de metalls (argent, or, estany, coure) a partir de minerals, i com emprar el mercuri en l’elaboració de diferents remeis medicinals. Els remeis clàssics rasayana tenen com a matèria primera minerals i gemes (inclosos biominerals: perles, corall), a banda de mercuri, i en les darreres dècades hom ha tendit a prescindir-ne, en part pel cost i en part per la conscienciació sobre la toxicitat del mercuri. Així, els remeis rasayana més estesos actualment es fan a partir d’un ventall de plantes medicinals (Emblica officinalis, Terminalia belerica, Terminalia chebula, etc.). Més enllà de la medicina, la rasayana influí en el seu temps en l’elaboració de pintures, en el tractament de la fusta, en la confecció d’acers, etc. Nosaltres arribem avui a l’element 80, centre de tota aquesta ciència.

Nagarjuna és considerat el fundador del “Madhyamaka”, doctrina intermèdia (“allò que sorgeix de manera dependent, declarem que és buit, que és una designació dependent, i que ell mateix és la via intermèdia”), i conegut també pels seus tractats sobre “l’essència del mercuri”
La descoberta del mercuri
El coneixement del mercuri s’enfonsa en l’albada de l’anomenada “Edat dels Metalls”. Els primers metal•lúrgics de Xina o Índia el devien conèixer ja fa més de 4 mil•lennis. Des d’un bon començament, a Xina o a Tibet, se li atribuïren propietats medicinals, des de les més genèriques (conservació de la salut, extensió de la vida) a les més concretes (guarir de fractures òssies, etc.). Aquestes aplicacions medicinals s’havien de fer amb molta cura, car els vapors d’aquest metall líquid podien produir efectes indesitjables.

El cinabre fou utilitzat des del neolític com a pedra ornamental i com a pigment. A l’Àsia sud-occidental se l’utilitzà com a cosmètic. El cinabre també esdevingué la principal font mineral de mercuri
Les dades arqueològiques indiquen ja la presència de mercuri en tombes egípcies del segle XIV a.e.c. El cinabre, mineral del qual era extret, també era utilitzat com a cosmètic. Alhora, el mercuri entrava en la formulació de diversos cosmètics i ungüents medicinals.
A partir de la segona meitat del I mil•lenni a.e.c. es generalitza a la Conca Mediterrània l’ús del mercuri en metal•lúrgia. El mercuri era emprat per formar amalgames amb altres metalls.
En diferents cultures, aquest metall era concebut com una forma d’argent líquid, bo i reconeixent que es tractava d’una substància diferent de l’argent. En japonès, hom parla de 水銀 (argent d’aigua) i de manera similar en grec se l’anomena “ΰδραργυρος”. En d’altres llengües, hom parla d’argent viu, i aquest era el nom originari en llatí (“argentum vivum”), mentre que en les llengües germàniques aquesta mateixa etimologia dóna lloc a “quicksilver” i construccions similars, o en llengües bàltiques a “gyvsidabris”. L’arrel persa “zhivah”, derivada de “viu”, és manllevada per diverses llengües (àrab, turc, llengües sud-eslaves). En hebreu se l’anomena “kesef” i ja hem vist abans el nom en sànscrit (rasa; que en indonesi torna “raksa”). En nàhuatl és “yoliamochitl” i en quítxua “yaku qullpi” o “puriq qullpi”.
Teofrast, en la seva obra sobre els minerals (315-314 a.e.c.), ens explica com s’obtenia hidrargent a partir d’esmicolar cinabri en un morter de coure (amb mà de morter també feta de coure).
Hom explica que Qin Shi Huang (260-210 a.e.c.), el primer emperador Qin, era ben familiaritzat amb les propietats de l’argent líquid. Els seus metges l’administraren pocions fetes amb aquest material i pols de jade per garantir-li una vida eterna o una joventut eterna. Però justament la seva mort, a 50 anys, és atribuïda als efectes de toxicitat crònica del mercuri, que li haurien afectar el fetge i potser el cervell. Naturalment, els seus metges descartaren cap relació i, de fet, en la tomba de Qin, en la qual es representa un model de l’imperi que havia aixecat, en la qual els rius eren representats per cursos de mercuri.
També la medicina greco-llatina era interessada en l’hidrargent. Així apareix citat en l’obra de Dioscòrides, que explica com obtindre mercuri a partir de la destil•lació de cinabri en recipients de ferro. Les principals mines de l’Imperi Romà eren a les actuals Almadén i al Monte Amiata. De la producció romana de cinabri, la part principal es destinava a la transformació en colorant i només una part menor a la destil•lació d’hidrargent. Plini parla de l’“argent viu” en el capítol 32 del Volum XXXIII d’Historia Naturalis. Plini parla, entre d’altres coses, de la fragilització que l’argent viu provoca en diversos metalls.
Fa uns mesos, sota el Temple de Quetzalcoatl, la tercera piràmide més gran de Teotihuacan (construïda l’any 200 e.c.), hom trobà una cambra a 20 metres de fondària amb grans quantitats de mercuri. En la ciutat maia de Lamanai hom trobà una piscina de mercuri sota una pista cerimonial de joc.
En la tradició alquímica, l’hidrargent és considerat com la matèria primera comuna als diferents metalls sòlids. En una d’aquestes explicacions, els metalls eren considerats la barreja entre un principi fluid i un principi inflamable, amb l’or com el més nobles i el plom com el més baix.
Segons una altra interpretació, el nombre de metalls era set, i l’hidrargent era considerat un d’ells. Aquesta llista de set metalls facilitava la identificació amb els set planetes, que havien rebut nom a partir de set divinitats gregues. L’hidrargent era identificat amb el planeta Hermes, que en llatí era denominat Mercuri i en llengües semítiques Utarid. La identificació era afavorida pel fet que, dels planetes puntuals, Mercuri és el d’òrbita més ràpida i inquieta. A partir del déu Utarid s’explicaria l’arrel “rtut” que trobem per designar el mercuri en diferents llengües eslaves. En no poques llengües, hi ha un equilibri entre el nom clàssic i el nom planetari d’aquest metall líquid. No és pas el cas del català, on domina clarament “mercuri”. En anglès, “quicksilver” és en clar retrocés, com ho és “azogue” (derivat d’un mot àrab) en castellà. Actualment, en gujarati hom parla de “મર્ક્યુરી” (markyuri). D’aquesta identificació deriva l’ús de ☿ com a símbol d’aquest metall líquid.
Jabir ibn Jayyan (721-815 e.c.) refundava l’alquímia, amb una orientació més nítidament experimental. En la part teòrica, Jabir transformava la doctrina dels quatre elements clàssics, en reconèixer la materialitat de l’èter, i de dos principis addicionals: la combustibilitat (associada al sofre) i la metal•licitat (associada amb el mercuri). Les amalgames en mercuri adquirien un paper central en la recerca sobre la crisopeia, la transmutació en or de metalls baixos. Es simptomàtic el nom d’Almadén (la Mina) per referir-se a uns dels centres de producció de mercuri més importants del món, que va veure en mans de Castella en el 1151, que la confià a l’Orde militar de Calatrava.
En l’esquema alquímic de Paracels (1493-1541), el mercuri era un dels “tria prima”, concretament el principi fluid. Més tard, amb Johann Joachim Becher (1635-1682), aquest principi seria identificat més genèricament amb els metalls (“terra fluida”). Paracels és potser el nom més conegut de la iatroquímica, és a dir de l’aplicació de l’alquímia en la sanació. El mercuri fou prescrit per a la sífilis, malaltia que esdevingué endèmica a Europa en aquelles dècades. Malaltia crònica de transmissió sexual, s’atribueix a Paracels la dita segons la qual “n’hi ha prou amb una nit amb Venus per haver de passar tota una vida amb Mercuri”.

Wankawilka (Huancavelica) fou fundada el 5 d’agost del 1572 pel virrei del Perú, Francisco de Toledo. El 1563, Nahuincopa, servidor de Jerónimo Luís de Cabrera hi va descobrir mines de mercuri. El mercuri de Wankawilka, extret dificultosament dels “socavones” suplí les necessitat d’aquest metall líquid per a les mines d’argent, fins al punt que en 1648 un virrei afirmava que “Potosí i Huancavelica són els dos pilars en els quals recolza aquest reialme del Perú i el d’Espanya”. En el decurs de tres segles d’explotació, s’extragueren de Huancavelica 100.000 tones de mercuri
La introducció de noves tècniques metal•lúrgiques a Europa en el segle XVI d’amalgamació augmentaren la demanda de mercuri. A les Amèriques, el processament de mineral d’or i d’argent (invenció del procés “patio” en el 1554 per Bartolomé de Medina a Pachuca, Nova Espanya) demanava unes quantitats de mercuri que no podien satisfer les mines d’aquell continent. Així, la major part del mercuri d’Almadén era exportat, via Sevilla, a Amèrica (les mines de mercuri de Huancavelica, Perú, no serien descobertes fins el 1563). Les riqueses d’or i d’argent per a l’Imperi Espanyol revolucionaren l’economia europea. Els banquers de l’emperador Carles V havien guanyat poder a través dels seus préstecs a la monarquia hispànica. Eventualment, la gestió de les mines d’Almadén passà a mans de la casa Fugger d’Augsburg. A partir del 1566, davant la insuficiència de la producció, el rei Felip II subministrà als Fugger presoners forçat a treballar a Almadén. Els diferents reports de l’època mostren els efectes sobre la salut de l’exposició crònica al mercuri. Als forzados s’uniren després esclaus nord-africans que, en el 1613, ja suposava la majoria de mà d’obra a Almadén. En el 1645, conclogué la concessió dels Fugger, i la corona es va fer càrrec directe de la gestió. A final del segle XVIII, treballadors lliures desplaçaren esclaus i forçats a Almadén, a la vegada que s’introduïen innovacions mineres. El mercuri es guardava i transportava en recipients de ferro. Eventualment, els flascons estàndards de mercuri contenien una quantitat equivalent a 34,46 quilograms de mercuri.

Termòmetre de mercuri. El caràcter líquid, la densitat i el coeficient d’expansió tèrmica, feren interessant el mercuri en l’elaboració d’aparells per mesurar la pressió (baròmetres) o la temperatura (termòmetres). Entrat en el segle XX, els termòmetres de mercuri deixarien pas als termòmetres d’alcohol (amb colorant vermell, o blau) i, més tard, als termòmetres electrònics
Definitivament considerat un metall simple (l’únic metall líquid en condicions estàndards), el mercuri és consignat com una de les substàncies simples en la taula de Lavoisier del 1789. En aquesta taula apareix senzillament amb el nom de “mercure”, juntament amb d’altres “substàncies simples metàl•liques oxidables o acidificables”.

Alguns dels símbols químics emprats per John Dalton en el 1808. El mercuri (10) apareix simbolitzat amb una corona en la qual s’insereixen vuit cercles. Hom representa així les gotes rodones de mercuri
En el sistema de símbols químics de Berzelius, el mercuri és simbolitzat Hg, a partir del mot llatí “hydrargyrum”. De vegades, hom també utilitzarà el símbol Hy, però finalment s’establirà Hg. Algunes llengües s’han estimat més emprar mots derivats d’“hidrargent” per no separar-se del símbol. Així, en esperanto, s’utilitza “hidrargo”.
La Banca Rotschild va adquirir la mina de mercuri d’Idrija (explotada des del 1490) i, en el 1835, va rebre la concessió indefinida d’Almadén. Això feia disposar als Rotschild de bona part de la producció de mercuri, la demanda del qual creixia al ritme de la industrialització.
Vers el 1846 hom es va fer conscient de la importància d’una mina de cinabri a Califòrnia, que Andrew Forbes batejà amb el nom de Nuevo Almadén. La mina ja havia estat explotada pels ohlones, per a la producció de pigment i, des del 1820, per part de colons mexicans per a la de mercuri. La titularitat de la mina fou disputada durant molt de temps entre Andrés Castillero i la Barron-Forbes Company, que va ensortir-se’n amb la gestió. Aquesta querella judicial, va fer que Lincoln, en el 1863, en plena guerra civil, provés de nacionalitzar-la, però topà amb l’oposició dels miners. Tot i així, la Barron-Forbes accedí a vendre-la a inversors americans. De llavors ençà, New Almaden esdevingué un gran centre de producció, que serví alhora a la producció aurífera de Califòrnia. El control dels Rotschild declinava, més encara quan l’Almadén original retornava a titularitat estatal espanyola (1863).
En el 1865 s’aconseguí la síntesi del primer compost organo-mercúric, el dimetilmercuri. La toxicitat d’aquest producte era extrema i, de fet, dos ajudants de laboratori van morir-se setmanes després de la síntesi.
Els intents de sistematitzar els elements químics comencen particularment amb John Newlands, el 1864. En el seu sistema el mercuri (Hg) rep el nombre 52, i és inclòs en el grup del glucini (=beril•li).
Més popular seria la taula periòdica de Mendeleev. En la de 1869, el mercuri (Hg = 200) apareix en el sisè període, dins del grup de l’hidrogen, el coure i l’argent. En la taula del 1871, passà a l’onzè període, dins del grup II (el grup del beril•li). Dissenys ulteriors, ja entrat el segle XX, el traslladaran de nou al sisè període, ara situat el grup del zinc i del cadmi.

Pot de sublimat corrosiu (biclorur de mercuri). Aquesta substància era emprada com a preservador per a mostres biològiques en el segle XIX. La medicina àrab l’utilitzà per a desinfectar ferides fins entrat el segle XX
El pic de producció de la mina d’Almadén s’assolí el 1941, amb 2800 tones de mercuri. La caiguda del preu del mercuri (el 1976 havia caigut a un 20% del valor del 1965) motiva el tancament de no poques mines històriques. Fou el cas de New Almaden, que tancà el 1976, després d’una producció total estimada de 38090 tones. La recerca d’alternatives menys contaminants va reduir la demanda industrial de mercuri, de manera que el preu continuà davallant. En el 2000, tancava la mina d’Almadén, convertida llavors, com New Almaden, en museus.

Estructura química de la merbromina (dibromhidromercurifluorosceïna sal sòdica). És un sòlid de color verd fosc. És fàcilment soluble en aigua. Les solucions concentrades (0,5%) són de color vermell carmí i les més diluïdes (1:2000) incolores, però encara amb una fluorescència groc-verdosa. Emprat com a antisèptic d’ús tòpic en petites ferides, fou comercialitzat a casa nostra amb el nom registrat de “mercromina” a partir del 1935
El 21 d’abril del 1956 ingressà a l’Hospital de la Fàbrica Chisso, a Minamata (Kumamoto, Kyushu, Japó) una nena de cinc anys, amb una quadre de dificultats locomotrius, en la parla i amb convulsions. El dia 23 ingressava encara una germana petita, amb el mateix quadre. Llavors la mare de les nenes va comunicar que la filla d’uns veïns mostrava símptomes més semblants. Es va fer una visita a la cases del veïnat, trobant-hi vuit persones amb aquests quadres, que foren ingressades. L’1 de maig, el director de l’hospital comunicava a l’oficina local de salut pública la descoberta d’“una epidèmia de malaltia desconeguda del sistema nerviós central”. A final de mes s’instituí un Comitè de Mesures contra l’estranya malaltia. Hom sospità d’una malaltia contagiosa i es prengueren les mesures oportunes, però eventualment es descartà el contagi, tot i que a aquelles alçades les persones afectades ja van quedar estigmatitzades per molts anys. En el decurs de les investigacions, els veïns parlaren de la “malaltia del gat ballador”, que havien patit diversos gats des dels anys 1950, amb un quadre de convulsions i comportaments estranys, eventualment letal. També reportaven la mort de corbs en ple vol, l’absència d’algues en el litoral i peixos que hi suraven morts. El 24 d’agost, es formava un Grup de Recerca a la Universitat de Kumamoto. Pels volts d’octubre, el nombre de casos registrats eren 40 persones, 14 de les quals s’havien mort. Les famílies vivien en el litoral de la badia, de la qual consumien com a alimentació bàsica peix i marisc. Els investigadors pensaren en una intoxicació alimentària. El 4 de novembre ja comunicaven que “la malaltia de Minamata la consideren més aviat una intoxicació per metall pesant, que presumiblement entra en el cos humà principalment a través del peix i del marisc”.
El veredicte científic assenyala a les aigües residuals de la planta Chisso. Aquesta planta química havia estat oberta en el 1908. Un dels seus principals productes era acetaldehid (6000 tones anuals en el 1951), per a la producció del qual s’utilitza sulfat de mercuri i sulfur fèrric com a catalitzadors. Els abocaments de Chisso ja havien generat problemes a la Badia de Minamata, que havien conduït en 1926 i en 1943 a indemnitzacions en benefici de la cooperativa de pescadors. A Minamata, el 25% dels llocs de feina els fornia Chisso, així com el 50% dels ingressos municipals. Els abocament, efectivament, contenien concentracions elevades de plom, mercuri, manganès, arsènic, tal•li, coure i seleni. Veritablement, hi havia concentracions elevades de manganès en les mostres d’òrgans de les persones que havien mort de la malaltia i en peixos de Minamata. D’altres sospitaven més aviat del tal•li, o del seleni, o fins i tot d’una combinació de contaminants. Douglas McAlpine (1890-1981) suggerí en visitar la zona, el març del 1958, que els símptomes li recordaven enverinament amb mercuri orgànic. El febrer del 1959 començà un estudi sobre la distribució de mercuri a la Badia. Es mostrà que les concentracions més elevades eren en el canal d’aigües residuals de Chisso en el port de Hyakken (concentracions de 0,2% de mercuri en el sediment!). Els nivells de mercuri en el veïns de Minamata tenien una concentració mitjana de 191 ppm (4 ppm és el valor habitual en altres zones del Japó), que arribava a 705 ppm en un dels pacients. El novembre del 1959, el Subcomitè creat pel ministeri de Salut i Benestar presentava la conclusió sobre la responsabilitat de Chisso. En aquella època la fàbrica produïa 45.000 tones anuals d’acetaldehid. La combinació de sulfat de mercuri i de sulfur fèrric, emprada des d’agost del 1951, resultava inadvertidament en la producció de mercuri orgànic, concretament metilmercuri. Chisso arribà a un tercer acord de compensacions amb els pescadors i els pacients, no sense una lluita enèrgica de la cooperativa de pescadors durant l’agost del 1959. La pol•lució continuà. En els anys següent es va descriure la malaltia congènita de Minamata. En el 1965 hi hagué un brot de malaltia de Minamata al riu Agano (Niigata, Honshu, Japó), per les mateixes causes. L’empresa responsable d’aquest cas, però, Showa Denko, no era pas tan poderosa localment, i els pacients tingueren resposta més aviat en les seves reivindicacions. Fins el setembre del 1968, Chisso no aturà la producció d’acetaldehid amb ús de catalitzador de mercuri.
Casos com el de Minamata estimularen arreu del món la investigació sobre la toxicologia del mercuri i dels metalls pesants. Una d’aquestes investigadores fou Karen Wetterhahn (*Plattsburgh, NY, 16.10.1948). Amb més de 85 publicacions a l’esquena, el 14 d’agost del 1996 realitzava experiments sobre la interacció d’ions mercuri i cadmi amb les proteïnes de reparació d’ADN. Com a material de referència emprava dimetilmercuri. En un de les pipetejades, li caigueren una o dues gotes de dimetilmercuri sobre el guant de làtex. No li va donar cap importància. Tres mesos després, Wetterhahn començà a patir molèsties abdominals i s’adonà que havia perdut força pes. El gener del 1997 ingressà amb pèrdua d’equilibri i trastorns de la parla. Les proves diagnosticaren una intoxicació amb mercuri. Els nivells sanguinis eren de 4 mg/L, 80 vegades superiors al llindar tòxic. El contingut urinari era de 0,234 mg/L (a partir de 0,05 és indici de toxicitat). Wetterhahn va ser tractada amb agents quelants. Els nivells coincidien amb els resultants d’una única exposició a dimetilmercuri, i recerques posteriors mostraren com els guants eren una protecció insuficient per al dimetilmercuri. Tres setmanes després de l’ingrés, queia en coma, i es moriria el 8 de juny del 1997.
El mercuri: isòtops i abundància
La massa atòmica estàndard del mercuri és de 200,592 uma, que resulta de la mitjana ponderada dels seus isòtops naturals (202Hg, 200Hg, 199Hg, 201Hg, 198Hg, 204Hg, 196Hg). La llista completa d’isòtops fa:
– mercuri-171 (171Hg; 171,00376 uma). Nucli format per 80 protons i 91 neutrons. És un isòtop molt inestable, amb una semivida de 8•10-5 s.
– mercuri-172 (172Hg; 171,99883 uma). Nucli format per 80 protons i 92 neutrons. És un isòtop molt inestable, amb una semivida de 4,2•10-4 s.
– mercuri-173 (173Hg; 172,99724 uma). Nucli format per 80 protons i 93 neutrons. És un isòtop molt inestable, amb una semivida de 0,0011 s.
– mercuri-174 (174Hg; 173,992864 uma). Nucli format per 80 protons i 94 neutrons. És un isòtop molt inestable, amb una semivida de 0,002 s.
– mercuri-175 (175Hg; 174,99142 uma). Nucli format per 80 protons i 95 neutrons. És un isòtop molt inestable, amb una semivida de 0,0108 s. Decau a platí-171, amb emissió d’un nucli d’heli-4.
– mercuri-176 (176Hg; 175,987355 uma). Nucli format per 80 protons i 96 neutrons. És un isòtop molt inestable, amb una semivida de 0,0204 s. Decau normalment (98,6%) a platí-172 (amb emissió d’un nucli d’heli-4) o, alternativament (1,4%), a or-176 (amb emissió d’un positró).
– mercuri-177 (177Hg; 176,98628 uma). Nucli format per 80 protons i 97 neutrons. És un isòtop molt inestable, amb una semivida de 0,1273 s. Decau majoritàriament (85%) a platí-173 (amb emissió d’un nucli d’heli-4) o, alternativament (15%), a or-177 (amb emissió d’un positró).
– mercuri-178 (178Hg; 177,982483 uma). Nucli format per 80 protons i 98 neutrons. És un isòtop molt inestable, amb una semivida de 0,269 s. Decau majoritàriament (70%) a platí-174 (amb emissió d’un nucli d’heli-4) o, alternativament (30%), a or-178 (amb emissió d’un positró).
– mercuri-179 (179Hg; 178,981834 uma). Nucli format per 80 protons i 99 neutrons. És un isòtop inestable, amb una semivida de 1,09 s. Decau bé a platí-175 (53%; amb emissió d’un nucli d’heli-4), a or-179 (47%; amb emissió d’un positró) o a platí-178 (0,15%; amb emissió d’un protó i d’un positró).
– mercuri-180 (180Hg; 179,978266 uma). Nucli format per 80 protons i 100 neutrons. És un isòtop inestable, amb una semivida de 2,58 s. Decau bé a or-180 (52%; amb emissió d’un positró) o a platí-176 (48%; amb emissió d’un nucli d’heli-4). Quan se’l sintetitza a partir de tal•li-180, a més, pot patir una fissió espontània asimètrica i donar lloc a ruteni-100 i criptó-80 (Andreyev et al., 2010).
– mercuri-181 (181Hg; 180,977819 uma). Nucli format per 80 protons i 101 neutrons. És un isòtop inestable, amb una semivida de 3,6 s. Decau bé a or-181 (64%; amb emissió d’un positró), a platí-177 (36%; amb emissió d’un nucli d’heli-4), a platí-180 (0,014%; amb emissió d’un protó i d’un positró) o a iridi-177 (0,000009%; amb emissió d’un nucli d’heli-4 i d’un positró). Posseeix un estat metastable (181mHg) a 210 keV.
– mercuri-182 (182Hg; 181,97469 uma). Nucli format per 80 protons i 102 neutrons. És un isòtop inestable, amb una semivida de 10,83 s. Decau majoritàriament (84,8%) a or-182 (amb emissió d’un positró) o, alternativament, a platí-178 (15,2%; amb emissió d’un nucli d’heli-4) o a platí-181 (0,00001%; amb emissió d’un protó i d’un positró).
– mercuri-183 (183Hg; 182,974450 uma). Nucli format per 80 protons i 103 neutrons. És un isòtop inestable, amb una semivida de 9,4 s. Decau majoritàriament (74,5%) a or-183 (amb emissió d’un positró) o, alternativament, a platí-179 (25,5%; amb emissió d’un nucli d’heli-4) o a platí-182 (0,00056%; amb emissió d’un protó i d’un positró). Posseeix dos estats metastables, un a 198 keV (183m1Hg) i un altre a 240 keV (183m2Hg; que té una semivida de 5 s).
– mercuri-184 (184Hg; 183,971713 uma). Nucli format per 80 protons i 104 neutrons. És un isòtop inestable, amb una semivida de 30,6 s. Decau normalment (98,89%) a or-184 (amb emissió d’un positró) o, alternativament (1,11%), a platí-180 (amb emissió d’un nucli d’heli-4).
– mercuri-185 (185Hg; 184,971899 uma). Nucli format per 80 protons i 105 neutrons. És un isòtop inestable, amb una semivida de 49,1 s. Decau majoritàriament (94%) a or-185 (amb emissió d’un positró) o, alternativament (6%), a platí-181 (amb emissió d’un nucli d’heli-4). Posseeix un estat metastable (185mHg) a 99,3 keV, que té una semivida de 21,6 s, i que decau bé a l’estat basal (54%) o a or-185 (46%) o a platí-181 (0,03%).
– mercuri-186 (186Hg; 185,969362 uma). Nucli format per 80 protons i 106 neutrons. És un isòtop inestable, amb una semivida de 82,8 s. Decau normalment (99,92%) a or-186 (amb emissió d’un positró) o, alternativament (0,016%), a platí-182 (amb emissió d’un nucli d’heli-4). Posseeix un estat metastable (186mHg) a 2217,3 keV, que té una semivida de 8,2•10-5 s.
– mercuri-187 (187Hg; 186,969814 uma). Nucli format per 80 protons i 107 neutrons. És un isòtop inestable, amb una semivida de 114 s. Decau normalment a or-187 (amb emissió d’un positró) o, alternativament (0,00012%), a platí-183 (amb emissió d’un nucli d’heli-4). Posseeix un estat metastable (187mHg) a 59 keV, que té una semivida de 140 s, i que decau bé a or-187 o a platí-183 (0,00025%).
– mercuri-188 (188Hg; 187,967577 uma). Nucli format per 80 protons i 108 neutrons. És un isòtop inestable, amb una semivida de 195 s (3 minuts). Decau normalment a or-188 (amb emissió d’un positró) o, alternativament (0,000037%), a platí-184 (amb emissió d’un nucli d’heli-4).
– mercuri-189 (189Hg; 188,96819 uma). Nucli format per 80 protons i 109 neutrons. És un isòtop inestable, amb una semivida de 460 s (8 minuts). Decau normalment a or-189 (amb emissió d’un positró) o, alternativament (0,00003%), a platí-185 (amb emissió d’un nucli d’heli-4). Posseeix un estat metastable (189mHg) a 80 keV, que té una semivida de 520 s, i que decau a or-189 o a platí-185 (0,00003%).
– mercuri-190 (190Hg; 189,966322 uma). Nucli format per 80 protons i 110 neutrons. És un isòtop inestable, amb una semivida de 1200 s (20 minuts). Decau normalment a or-190 (amb emissió d’un positró) o, alternativament (0,00005%), a platí-186 (amb emissió d’un nucli d’heli-4).
– mercuri-191 (191Hg; 190,967157 uma). Nucli format per 80 protons i 111 neutrons. És un isòtop inestable, amb una semivida de 2900 s (49 minuts). Decau a or-191 (amb emissió d’un positró). Posseeix un estat metastable (191mHg) a 128 keV, que té una semivida de 3050 s i que decau a or-191, amb emissió d’un positró.
– mercuri-192 (192Hg; 191,965634 uma). Nucli format per 80 protons i 112 neutrons. És un isòtop inestable, amb una semivida de 1,75•104 s (5 hores). Decau a normalment a or-192 (per captura electrònica) o, alternativament (0,000004%), a platí-188 (amb emissió d’un nucli d’heli-4).
– mercuri-193 (193Hg; 192,966665 uma). Nucli format per 80 protons i 113 neutrons. És un isòtop inestable, amb una semivida de 1,37•104 s (4 hores). Decau a or-193, amb emissió d’un positró. Posseeix un estat metastable (193mHg) a 140,76 keV, que té una semivida de 4,25•104 s, i que decau bé a l’estat basal (7,1%) o a or-193 (92,9%).
– mercuri-194 (194Hg; 193,965439 uma). Nucli format per 80 protons i 114 neutrons. És un isòtop inestable, amb una semivida de 1,40•1010 s (444 anys). Decau a or-194, per captura electrònica.
– mercuri-195 (195Hg; 194,966720 uma). Nucli format per 80 protons i 115 neutrons. És un isòtop inestable, amb una semivida de 3,791•104 s (11 hores). Decau a or-195, amb emissió d’un positró. Posseeix un estat metastable (195mHg) a 176,07 keV, que té una semivida de 1,50•105 s, i que decau bé a l’estat basal (54,2%) o a or-195 (45,8%).
– mercuri-196 (196Hg; 195,965833 uma). Nucli format per 80 protons i 116 neutrons. Teòricament, decau a platí-192 (amb emissió d’un nucli d’heli-4) o a platí-196 (amb emissió de dos positrons). Ho faria, però, amb una semivida tan llarga, de 7,9•1025 s (vuit ordres de magnitud superior a l’edat actual de l’univers) que, a efectes observacionals, és un isòtop estable. La freqüència isotòpica és de 0,15%.
– mercuri-197 (197Hg; 196,967213 uma). Nucli format per 80 protons i 117 neutrons. És un isòtop inestable, amb una semivida de 2,309•105 s (64 hores). Decau a or-197, per captura electrònica. Posseeix un estat metastable (197mHg) a 298,93 keV, que té una semivida de 8,57•104 s, i que decau bé a l’estat basal (91,4%) o a or-197 (8,6%).
– mercuri-198 (198Hg; 197,9667690 uma). Nucli format per 80 protons i 118 neutrons. Teòricament, decau a platí-194, amb emissió d’un nucli d’heli-4. Ho faria, però, amb una semivida tan llarga que, a efectes observacionals, és un isòtop estable. La freqüència isotòpica és de 9,97%.
– mercuri-199 (199Hg; 198,9682799 uma). Nucli format per 80 protons i 119 neutrons. Teòricament, decau a platí-195, amb emissió d’un nucli d’heli-4. Ho faria, però, amb una semivida tan llarga que, a efectes observacionals, és un isòtop estable. La freqüència isotòpica és de 16,87%. Posseeix un estat metastable (199mHg) a 532,48 keV, que té una semivida de 2560 s i que decau a l’estat basal.
– mercuri-200 (200Hg; 199,9683260 uma). Nucli format per 80 protons i 120 neutrons. Teòricament, decau a platí-196, amb emissió d’un nucli d’heli-4. Ho faria, però, amb una semivida tan llarga que, a efectes observacionals, és un isòtop estable. La freqüència isotòpica és de 23,10%.
– mercuri-201 (201Hg; 200,9703023 uma). Nucli format per 80 protons i 121 neutrons. Teòricament, decau a platí-197, amb emissió d’un nucli d’heli-4. Ho faria, però, amb una semivida tan llarga que, a efectes observacionals, és un isòtop estable. La freqüència isotòpica és de 13,18%. Posseeix un estat metastable (201mHg) a 766,22 keV, que té una semivida de 9,4•10-5 s.
– mercuri-202 (202Hg; 201,9706430 uma). Nucli format per 80 protons i 122 neutrons. Teòricament, decau a platí-198, amb emissió d’un nucli d’heli-4. Ho faria, però, amb una semivida tan llarga que, a efectes observacionals, és un isòtop estable. La freqüència isotòpica és de 29,86%.
– mercuri-203 (203Hg; 202,9728725 uma). Nucli format per 80 protons i 123 neutrons. És un isòtop inestable, amb una semivida de 4,0258•106 s (47 dies). Decau a tal•li-203, amb emissió d’un electró. Posseeix un estat metastable (203mHg) a 933,14 keV, que té una semivida de 2,4•10-5 s.
– mercuri-204 (204Hg; 203,9734939 uma). Nucli format per 80 protons i 124 neutrons. Teòricament, decau a platí-200 (amb emissió d’un nucli d’heli-4) o a plom-204 (amb emissió de dos electrons). Ho faria, però, amb una semivida tan llarga que, a efectes observacionals, és un isòtop estable. La freqüència isotòpica és de 6,87%.
– mercuri-205 (205Hg; 204,976073 uma). Nucli format per 80 protons i 125 neutrons. És un isòtop inestable, amb una semivida de 308 s (5 minuts). Decau a tal•li-205, amb emissió d’un electró. Posseeix un estat metastable (205mHg) a 1556,4 keV, que té una semivida de 0,00109 s i que decau a l’estat basal.
– mercuri-206 (206Hg; 205,977514 uma). Nucli format per 80 protons i 126 neutrons. És un isòtop inestable, amb una semivida de 489 s (8 minuts).
– mercuri-207 (207Hg; 206,98259 uma). Nucli format per 80 protons i 127 neutrons. És un isòtop inestable, amb una semivida de 170 s (3 minuts). Decau a tal•li-207, amb emissió d’un electró.
– mercuri-208 (208Hg; 207,98594 uma). Nucli format per 80 protons i 128 neutrons. És un isòtop inestable, amb una semivida de 2500 s (42 minuts). Decau a tal•li-208, amb emissió d’un electró.
– mercuri-209 (209Hg; 208,99104 uma). Nucli format per 80 protons i 129 neutrons. És un isòtop inestable, amb una semivida de 37 s.
– mercuri-210 (210Hg; 209,99451 uma). Nucli format per 80 protons i 130 neutrons. És un isòtop inestable, amb una semivida de 600 s (10 minuts).
L’energia d’ionització és una de les propietats que marquen la periodicitat dels elements químics. A cada període li correspon un pic d’energia d’ionització corresponent a un gas noble. Una excepció és el pic que representa el mercuri, amb la major energia d’ionització de tots els metalls. La raó d’això es troba en el fet que té complets tots els nivells electrònics ocupats en la configuració basal. En conseqüència, forma enllaços febles i, en condicions elementals, presenta uns punts de fusió i d’ebullició inusualment baixos per a un metall.
L’àtom neutre de mercuri conté 80 electrons, amb una configuració basal d’escorça de 1s22s22p63s23p63d104s24p64d104f145s25p65d106s2. És, doncs, l’element del període 6 del grup 12 (el grup de zinc, els anomenats “metalls volàtils”), dins de bloc d (“metalls de transició”). Els estats d’oxidació més habituals són +2 (Hg2+; catió mercúric) i, en menor grau, +1 (Hg+, catió mercuriós). També és present en +4 (ex. HgF4) i 0. El radi atòmic és de 1,51•10-10 m.

Abocament de mercuri en una placa de Petri
En condicions estàndards de pressió i de temperatura, el mercuri es presenta com un líquid metàl•lic de color argentí. La densitat en aquestes condicions és de 13534 kg•m-3. Descomptant el brom, en l’única substància elemental que és en estat líquid en condicions estàndards.

Recipient amb mercuri elemental. Una moneda d’una lliura (densitat de 6700 kg•m-3) sura damunt del mercuri (densitat de 13534 kg•m-3), en part també per la tensió superficial del metall líquid. Observeu que, a diferència de l’aigua, el mercuri genera un menisc convex, degut a que la interacció amb les parets del vidre és menys forta que entre els àtoms de mercuri
En condicions estàndards de pressió, el mercuri solidifica a 234,3210 K.
En condicions estàndards de pressió, el mercuri bull a 629,88 K.
El mercuri no reacciona amb la majoria d’àcids. Sí ho fa amb àcids oxidants (àcid sulfúric concentrat, àcid nítric, aigua règia) donant lloc a les sals corresponents, com també amb àcid sulfhídric. El mercuri també reacciona amb sofre sòlid.
El mercuri es capaç de dissoldre, és a dir de formar amalgames, amb un ample ventall de metalls, com ara l’or, l’argent, el coure, el manganès, el zinc o l’alumini. No forma amalgama amb el ferro ni amb el platí.
Entre els compostos de mercuri podem esmentar:
– òxid. Cal exposar el mercuri a l’aire durant força temps a temperatura elevada, perquè es formi òxid mercúric (HgO; sòlid de color taronja, densitat de 11140 kg•m-3).
– halògens: Hg2Cl2 (sòlid de color blanc, densitat de 7150 kg•m-3), HgCl2 (sòlid de color blanc volàtil, conegut històricament com a “sublimat corrosiu”).
– hidrurs: HgH (gas incolor).
– sulfurs: HgS (sòlid, l’al•lòtrop α-Hg és de color vermell, i β-HgS de color negre).
– seleniür: HgSe (sòlid cristal•lí de color gris-negre).
– tel•luriür: HgTe (sòlid cristal•lí negre).
– compostos organomercúrics. El mercuri hi apareix sempre en valència II.

Òxid de mercuri (II)
L’abundància atòmica del mercuri en l’univers depèn de processos de nucleosíntesi que tenen lloc en estels madurs i en supernoves, i de l’estabilitat dels seus isòtops. El mercuri compta amb diversos isòtops quasi-estables, cosa que afavoreix la seva abundància, i que va lligat amb el fet de tindre un nombre atòmic parell. Per aquesta raó, el mercuri supera en abundància els dos elements que el flanquegen en la taula periòdica, l’or i el tal•li. A més, el mercuri, com els elements de nombres atòmics de 76 a 83, és més abundant que no pas esperaríem pel lloc que ocupa en la taula periòdica. Així, el mercuri és més abundant que un bon nombre d’elements més lleugers (tecneci, rodi, indi, antimoni, cesi, praseodimi, i els que van del nombre 61 al 75). Dels elements més pesants, tan sols el plom és més abundant.
En la Terra, l’abundància global del mercuri és de 0,02 ppm en termes de massa (0,003 ppm en termes atòmics). En l’escorça terrestre la concentració és superior a la mitjana, encara que limitada a 0,08 ppm en termes de massa. El mercuri és un element calcòfil, i així el trobem combinat a calcògens (oxigen, sofre, seleni, tel•luri). Hi ha minerals que arriben a concentracions de mercuri del 2,5%. És rar trobar-lo com a metall nadiu. El cinabri és el mineral de mercuri més comú, però també podem esmentar d’altres de molt més rars, com la corderoïta (Hg3S2Cl2), la livingstonita (HgSb4S8), el calomel (Hg2Cl2), la coloradoïta (HgTe), etc. Els minerals rics en mercuri apareixen sobretot en contexts geològics d’orogènia molt recent, amb roques d’alta densitat, i particularment en zones volcàniques o de fonts termals.
La concentració de mercuri en la hidrosfera varia segon els context geològic. En l’oceà, una concentració típica és de 30 μg•m-3.
La Glacera Frémont, a Nord-amèrica, ha estat estudiada pel que fa als nivells de mercuri en prospeccions del 1991 i del 1998. Segons l’antiguitat del glaç és possible fer un seguiment de la deposició històrica (expressada en mercuri total). Grans erupcions volcàniques com Tambora (1815), Krakatoa (1883) o Mt. St Helens (1880) generen pics aguts de deposició. A la segona meitat del segle XIX, dos pics s’associen a l’activitat minera desencadenada per les febres d’or nord-americanes de 1848 i 1884. La industrialització, especialment a partir del 1950, ha fet augmentar de manera gairebé permanent els nivells de deposició.
La presència de mercuri en l’atmosfera és transitòria, però constitueix una forma efectiva de transport. En atmosferes urbanes, la concentració típica és de 0,01-0,02 μg•m-3, però els valors pugen en llocs tancats.
El mercuri no és, segons se sap, bioelement per a cap organisme. La biosfera, però, pot absorbir i metabolitzar mercuri. La biometilació del mercuri juga un rol en el cicle geoquímic d’aquest element i, particularment, en l’agreujament de la contaminació d’aigües. La bioacumulació en la xarxa tròfica d’ecosistemes aquàtics afecta especialment als peixos situats en els nivells més alts, on pot acumular-se metilmercuri especialment en teixit muscular.
En el cos humà, una concentració típica en els nostres dies és de 0,19 ppm en termes de massa (0,089 ppm en termes atòmics), la qual cosa equival, per a un organisme de 70 kg, a 6 mg de mercuri total.
El mercuri elemental i els seus compostos són extremadament tòxics, si bé la major toxicitat la presenten els compostos orgànics (dimetilmercuri, mercuri). La facilitat d’absorció, fins i tot a través de pell i mucoses, n’afavoreix la toxicitat. L’exposició crònica a atmosferes de 0,7-42 μg•m-3 o l’exposició aguda a partir de 1100 μg•m-3 ja és suficient per presentar símptomes. El tractament de la intoxicació amb mercuri es realitza amb agents quelants com la N-acetil-penicil•lamina (NAP), l’anti-lewisita britànica (BAT), l’àcid 2,3-dimercapto-1-propanesulfònic (DMPS) o l’àcid dimercaptosuccínic (DMSA).
En casos de vessaments de mercuri, cal anar amb cura amb la recol•lecció, que es veu facilitada per la tendència de les gotes a fusionar-se. L’àrea afectada ha d’ésser després rentada amb pols (sofre, zinc, etc.) que formi amalgama amb mercuri.
El mercuri, avui
En les darreres setmanes ha circulat força aquest vídeo de Sofia Ashraf, que parla del moviment popular de Kodaikanal que reivindica que Unilever es faci càrrec de les operacions de neteja de la zona, molt afectada per la fàbrica de termòmetres i d’altres instruments de mercuri que hi fou activa fins el 2001
El 19 de gener del 2013 delegats de 140 estats signaven la Convenció de Minamata sobre el Mercuri, en el marc del Programa Ambiental de Nacions Unides (UNEP). En les darreres dècades hi ha hagut un esforç per trobar substituts al mercuri en les seves aplicacions industrials. Però és un procés força lent. A més, l’impacte ambiental de la mineria de mercuri o de la indústria que n’ha utilitzat perdura en els ecosistemes fins i tot dècades després d’haver-lo deixat de fer servir.
Actualment, la producció de mercuri és de 1600 tones anuals. La major part de la producció procedeix de l’Àsia central (Xina, Kirgízia), bàsicament de la mineria de cinabri. A Mèxic i a Xile, el mercuri apareix com a subproducte de l’electrorefinament del coure. A banda de la producció primària minera, hem de comptar amb el reciclatge de mercuri que és, a més, estimulat per les regulacions ambientals.
La reducció d’aplicacions industrials duria, en principi, el preu del mercuri cap a la baixa. Diversos factors, però, fan que el preu pateixi fortes oscil•lacions.
No totes les aplicacions del mercuri es troben en retrocés. El consum de mercuri en la confecció de làmpades continua a créixer. Les primeres làmpades de vapor de mercuri daten del 1901, i començaren a guanyar espai en els anys 1930, per exemple en la il•luminació de carrers.

Làmpada d’ultraviolat, emprada per a bronzejament artificial. En molts llocs és obligatori indicar des de fa anys que un tub fluorescent conté mercuri amb el signe Hg encerclat
De totes formes, el principal ús de mercuri encara es troba en la indústria química. El procés Castner-Kellner per a la producció de clor i sosa càustica a partir de NaCl empra un càtode de mercuri, on s’acumula el sodi que donarà lloc després a la sosa càustica. Des de mitjan dels anys 1980, aquest procés ha estat substituït per d’altres que no fan ús de l’elèctrode de mercuri.
Ja hem vist abans la llarga tradició d’aplicació del mercuri en medicina. Actualment, aquest ús és més limitat, però cal esmentar:
– l’ús de mercuri en odontologia. Les amalgames més habituals consisteixen en un 50% de mercuri, 22-32% d’argent, 14% d’estany, 8% de coure i d’altres metalls minoritaris. Factors estètics i consideracions sobre el mercuri han afavorit en algunes aplicacions l’ús de resines polimèriques. Tot i amb tot, compten també amb certs avantatges.
– el tiomersal és un compost organomercúric amb propietats antisèptiques. S’ha utilitzat com a preservatiu en vaccins, si bé hi ha una tendència en els darrers anys a disminuir-ne la concentració a prescindir-ne del tot.
– la merbromina (a casa nostra més coneguda com a “mercromina”) encara és utilitzada com a antisèptic en talls i esgarrinxades.
– en línies generals, tant en la medicina moderna com en les medicines tradicionals, hi ha una tendència a reduir la prescripció de fàrmacs amb compostos mercúrics. També es redueix el seu ús en instrumental mèdics (termòmetres, esfigmomanòmetres).
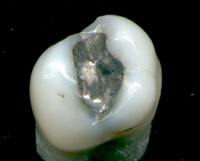
Dent tractada de càries amb una amalgama
D’altres aplicacions del mercuri o dels seus compostos són quantitativament menys rellevants:
– telescopis de mirall líquid. Clàssicament el líquid emprat ha estat el mercuri, però l’ús d’aliatges de gal•li amb baix punt de fusió (galinstan, etc.) podria desplaçar-lo.
– l’elèctrode de calomel (clorur de mercuri (I)) és emprat com a elèctrode de referència en electroquímica.
– en polarografia s’empren elèctrodes de mercuri
En les darreres dues dècades s’han decretat limitacions a l’ús de mercuri. Actualment, es calcular que de les emissions atmosfèriques de mercuri, tan sols la meitat són degudes a processos naturals (volcans, etc.). Pel que fa a les emissions antropogèniques, la principal font (65%) s’associa a centrals elèctriques que fa ús de combustibles fòssils, particularment de carbó. Són menors les contribucions d’altres processos industrials, com a la producció d’or (11%), la producció d’altres metalls (8,2%), la indústria del ciment (6,4%), etc. Val a dir un 3% de les emissions antropogèniques de mercuri es deuen a la incineració de residus, d’ací la importància de separar els residus que tenen continguts significatius de mercuri (bateries, làmpades fluorescents, productes químics, termòmetres i termòstats).
En ocasions, trobar substitut al mercuri ha resultat relativament fàcil. Ja fa temps que els termòmetres d’alcohol (freqüentment amb colorant vermell) van desplaçar a les cases als termòmetres de mercuri, tant en els termòmetres de paret com en els corporals. Més recentment, uns i altres són substituïts per termòmetres electrònics. Com a metall líquid, el mercuri pot ser substituït per aliatges de gal•li (galinstan) que també són líquid a temperatura estàndard. En d’altres casos, la reducció és paulatina, com s’esdevé en els termòstats, on hi ha hagut una reducció del mercuri per a la producció de cada unitat. En algunes circumscripcions s’han prohibit completament els productes que contenen deliberadament mercuri (Suècia, 2009).